O sangue contém uma proteína complexa chamada hemoglobina que transporta oxigênio dos pulmões para outras partes do corpo. Na doença genética conhecida como anemia falciforme, as moléculas de hemoglobina são anormais e têm solubilidade mais baixa, especialmente em sua forma não oxigenada. Consequentemente, até cerca de 85% da hemoglobina nos glóbulos vermelhos cristalizam na solução.
A razão para a insolubilidade da hemoglobina na anemia falciforme pode ser determinada por uma variação estrutural em cerca parte de uma cadeia lateral de aminoácido. As moléculas de hemoglobina normal têm aminoácido em sua construção com a seguinte cadeia lateral projetando-se do corpo principal da molécula:
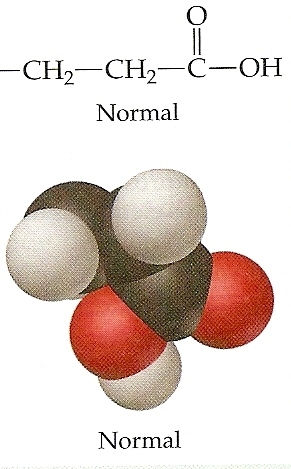
Essa cadeia lateral termina com um grupo polar, que contribui para a solubilidade da molécula de hemoglobina em água. Nas moléculas de hemoglobina de pessoas que sofrem de anemia falciforme, a cadeia lateral é de um tipo diferente:
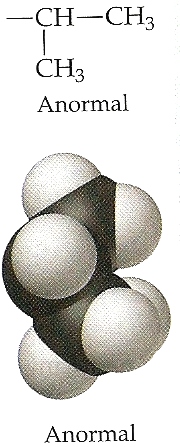
Esse grupo anormal de átomos é apolar (hidrofóbico), e sua presença leva à agregação dessa forma defeituosa de hemoglobina em partículas muito grandes para permanecer suspensas nos fluidos biológicos. Ela também faz com que as células se distorçam em forma de foice, como mostrado na Figura abaixo. As células em formato de foice obstruem as capilaridades, provocando dor intensa e deterioração gradual de órgãos vitais. A doença é hereditária e, se ambos os pais carregam genes defeituosos, é provável que os filhos possuam apenas hemoglobinas anormais.
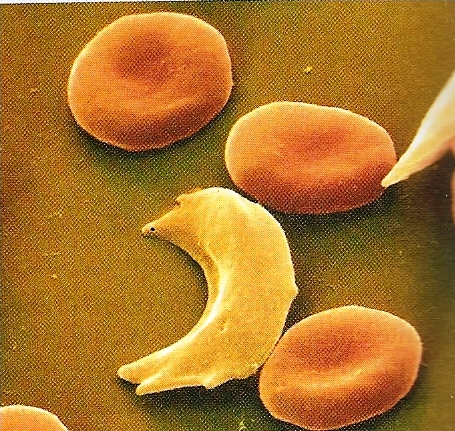
Figura acima: Micrografia obtida com microscópio eletrônico mostrando glóbulos vermelhos normais e glóbulos vermelhos falciformes.
Extraído: Química: A Ciência Central – 9ª edição.
