► Produto Iônico da Água (Kw):
Equação de auto-ionização da água:
.jpg)
► Constante de equilíbrio para a água:
.jpg)
► Caráter das soluções:
.jpg)
► Conceitos de pH e pOH:
Para evitar o uso de expressões matemáticas com expoentes negativos, o químico Sorensen propôs as seguintes definições:
pH ⇒ potencial hidrogeniônico, expressa a acidez em termos da concentração [H+]
pOH ⇒ potencial hidroxiliônico, expressa a bacisidade em termos da concentração [OH–]
.jpg)
Note que quanto maior for a acidez de uma solução, maior será [H+] e menor o pH!
.jpg)
Para ter facilidade nos cálculos envolvendo pH e pOH é importante que você recorde algumas propriedades de logarítmos: Veja então:
.jpg)
É importante saber que a molaridade das soluções é expressa em mols/L; M (molar), ou ainda [ ].
► Relação entre pH e pOH:
.jpg)
ATENÇÃO: Sempre considere a igualdade abaixo na hora de calcular o pH!
.jpg)
Lembre-se sempre que as soluções podem ser:
.jpg)
Exemplos de cálculo de pH:
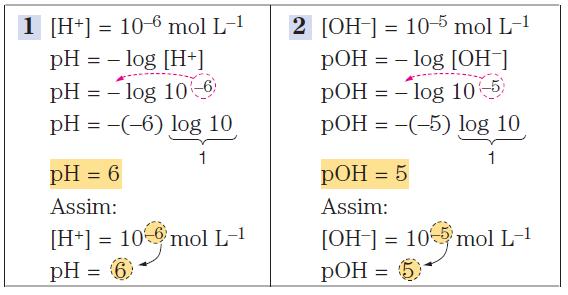
►Escala de pH e pOH:
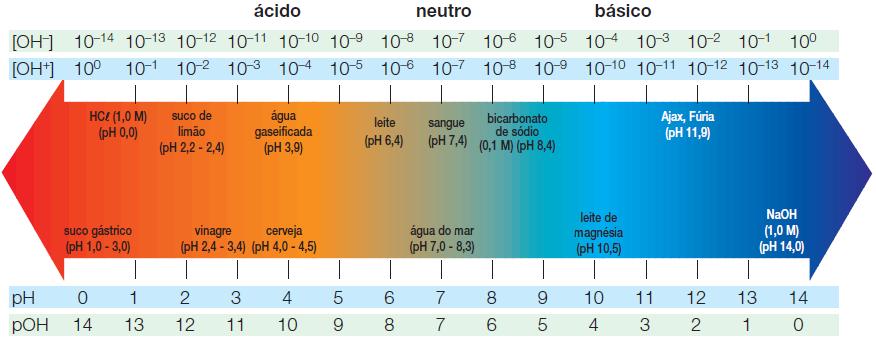
► Cálculo de pH para ácidos fracos (monoácidos):
– Soluções de monoácidos fracos (CH3COOH, HCN, HClO, etc)
.jpg)
Exemplo:

► Cálculo de pH para ácidos fortes:
– Solução de monoácido (H+) forte (HCl, HBr, HI, HNO3, etc)
.jpg)
Exemplo:

– Solução de diácido (2H+) forte (H2SO4, etc):
.jpg)
► Cálculo de pOH para bases fracas (monobases):
– Solução de monobase fraca (NH4OH):
Obs.: Recorde que o hidróxido de amônio é uma base extremamente fraca, mas altamente solúvel em água.
.jpg)
Exemplo:

► Cálculo de pOH para bases fortes:
– Solução de monobases fortes (NaOH, KOH, LiOH, etc). Lembre-se que as bases dos metais alcalinos são extremamentes fortes e solúveis.
.jpg)
Exemplo:

– Solução de dibases fortes (Ba(OH)2, Ca(OH)2, Sr(OH)2, etc). Lembre-se que as bases dos metais alcalinos-terrosos são fortes e razoavelmente solúveis, com EXCEÇÃO das bases Be(OH)2 e Mg(OH)2, que são fracas e praticamente insolúveis.
.jpg)
