
O ar puro apresenta uma composição em volume (ou em mol) aproximadamente igual a 20% de O2e 80% de N2. E a pressão parcial do gás O2 nessa mistura é dada pela expressão:
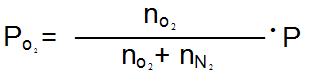
Estando ao nível do mar e, consequentemente, sujeito a uma pressão atmosférica igual a 101,3 kPa ou 1,01 • 105 Pa (1 atm), vejamos qual será a pressão parcial do gás O2 nessa situação:
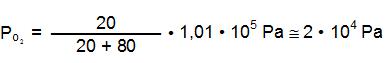
Dessa forma, podemos concluir que o organismo humano tem o seu melhor funcionamento quando a pressão parcial de O2¬ no ar for em torno de 2 • 104 Pa. Porém pode haver uma adaptação quando P02 estiver na faixa de 1 • 104 Pa a 6 • 104 Pa. É impossível a sobrevivência de um ser humano quando forçado a respirar fora desses limites. Analisemos, por exemplo, a situação de um mergulhador que está a uma profundidade de 30 metros e que leva consigo uma garrafa de ar comprimido O2 a 20% em volume. Nesse caso, a pressão exercida sobre ele é quatro vezes a da superfície, ou seja, 4,04 • 105 Pa. Assim:
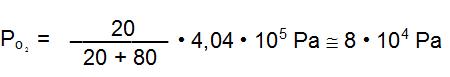
Nesse caso, a pressão parcial de O2 na mistura passa a ser 8 • 104 Pa, o que será fatal.
Outro problema que deve ser contornado é a presença de N2 na mistura. Caso sua pressão parcial seja superior a 1,01 • 105 Pa, ele se dissolverá apreciavelmente no sangue, provocando com o da embriaguez, denominado narcose de nitrogênio. Por essa razão, o nitrogênio é substituído pelo gás hélio, que, além de ser bem menos solúvel que o nitrogênio no sangue, não produz tal efeito.

Texto extraído de “INFORME-SE SOBRE A QUÍMICA”
Química: na abordagem do cotidiano, volume único/Francisco de Miragaia Peruzzo (Tito), Eduardo Leite do Canto. – 3.ed.- São Paulo: Moderna 2007.
