Algumas reações são muito rápidas, como é o caso da explosão da dinamite, enquanto outras são muito lentas, como é o caso da formação de estalactites (forma-se, em média, 1 cm a cada cem anos). A Cinética Química estuda a velocidade das reações químicas e os mecanismos pelos quais elas ocorrem.
Fatores que influenciam a velocidade
Para que uma reação química ocorra são necessárias duas condições indispensáveis: a afinidade química entre as substâncias e o contato entre elas. A explicação de como as reações ocorrem é dada pela Teoria do Complexo Ativado: no momento das colisões há um enfraquecimento progressivo das ligações entre as moléculas dos produtos. Entre o estado inicial (reagentes) e o final (produtos), temos um estado intermediário caracterizado pela formação de um complexo ativado.
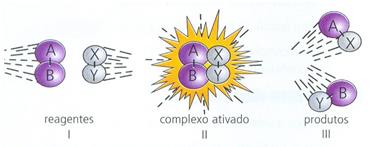
Podemos, portanto, concluir que a velocidade da reação depende da freqüência, da energia e da forma como os choques se processam. As condições extra-reação que podem ser manipuladas e, por conseqüência, afetar, os fatores acima citados, compõem as circunstâncias das quais dependem a velocidade da reação. Esses fatores são: estado de divisão, pressão, existência ou não de solução concentração dos reagentes, presença ou não de luz, presença ou não de catalisador.
• Energia de ativação
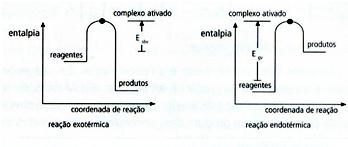
A energia utilizada para vencer a “resistência” dos reagentes, para levar os reagentes do estado inicial ao estado intermediário, caracterizado pela formação do complexo ativado, antes de se atingir o estado final, com a formação dos produtos da reação, é denominada energia de ativação. Energia de ativação é a energia mínima necessária para que as colisões entre as moléculas dos reagentes sejam eficazes, isto é, favoreçam a formação dos produtos. Quanto menor a energia de ativação maior a velocidade da reação.
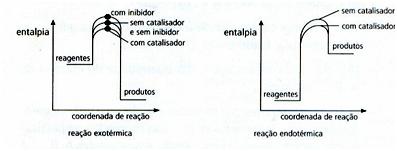
Um catalisador aumenta a velocidade da reação, pois diminui sua energia de ativação (um inibidor aumenta a energia de ativação).
Velocidade na Química
Numa reação química, a velocidade está relacionada ao tempo em que são consumidas quantidades de reagentes e formadas quantidades de produtos.
• Velocidade para uma substância
Considere uma substância S participando de uma reação, como reagente ou como produto:
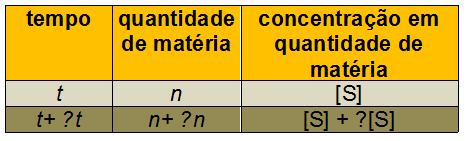
Se S for o produto da reação: ∆n > 0 e ∆ [S] > 0; se S for reagente: ∆n < 0 e ∆ [S] < 0.
Velocidade para uma reação
Considere a reação:
a A + b B + … → c C + d D + …
As velocidades de A, B, C, D, … são, respectivamente, Va, Vb, Vc, Vd, … Note que a relação entre as velocidades de duas substâncias quaisquer está na proporção dos coeficientes estequiométricos (Va / Vb = a/b; Vb, / Vd = b/d; …). A velocidade da reação (V) é definida por:
V = ( 1/a ) VA = ( 1/b ) VB = …( 1/c ) VC = (1/(d ) ) VD = …
Lei de Guldberg-Waage
Sabemos que quanto maior é a concentração dos reagentes maior é a velocidade da reação. A lei da Ação das Massas, ou lei de Guldberg-Waage, diz que: a velocidade de uma reação é diretamente proporcional ao produto das concentrações em quantidade de matéria dos reagentes, elevadas a determinados expoentes.
Para a reação química, realizada à temperatura t, a A + b B + … → produtos
a velocidade é dada por: V = K . [A]α . [B]β. … onde:
– K = constante de velocidade à temperatura t; ao aumentar a temperatura, K aumenta;
– α, β, … = expontes que só podem ser determinados experimentalmente; os números α, β, … são chamados, respectivamente, ordem da relação aos reagentes A, B, …; a ordem total da reação corresponde à soma de α + β + …
Meia-vida
Meia-vida é o tempo necessário para reagir a metade da quantidade de uma substância. É possível demonstrar que a meia-vida de uma reação de primeira ordem é constante e que seu valor está relacionado com a constante de velocidade por meio da expressão:
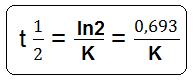
ATENÇÃO P/ ½
Reações elementares e complexas
Uma reação na qual todos os expoentes na equação da velocidade coincidem com os respectivos coeficientes estequiométricos da equação química é uma reação elementar; se um deles não coincidir, ela é uma reação complexa. Para a reação:
H2 (g) + I2 (g) → 2 Hl (g)
a velocidade da reação é dada por:
V = K . [H2] . [l2]
Portanto:
– ordem em relação ao H2 = 1;
– ordem em relação ao l2 = 1;
– ordem (total) da reação = 1 + 1 = 2;
– reação elementar (os dois expoentes coincidem com os coeficientes estequio-métricos).
Para a reação:
N2(g) + 3 H2(g) → 2 NH3(g)
A velocidade da reação (determinada experimentalmente) é dada por: V = K . [N2] . [H2]
Portanto:
– ordem em relação ao nitrogênio = 1;
– ordem em relação ao hidrogênio = 2;
– ordem (total) da reação = 1 + 2 = 3;
– reação complexa [o expoente do H2 (=2) não coincide com seu coeficiente (=3)].
Mecanismo das reações
Vimos que a velocidade é dada por: V = K. [A]α . [B]β …
– se α = a e β = b, a reação é elementar e se processa numa só etapa;
– se α ≠ a e/ou β ≠ b, a reação é complexa e se processa em várias etapas elementares; a velocidade da reação é igual à velocidade da etapa lenta (reação de menor velocidade).
A reação acima, do N2(g) com o H2(g), é complexa e acontece em duas etapas elementares.
N2(g) 2 H2(g) → N2H4(g), velocidade = V1
N2H4(g) + H2(g) → 2 NH3(g) velocidade = V2
N2(g) + 3 H2(g) → 2 NH3(g) velocidade = V3
Experimentalmente, verifica-se que V1 < V2 (a etapa lenta corresponde à reação). Dessa forma, pode-se escrever que V = V1 (a velocidade da reação complexa é igual à velocidade da reação elementar de menor velocidade) e não V = V1 + V2; então V = K . [N2] . [H2], pois na primeira reação o coeficiente do N2 é 1 e do H2 é 2.
