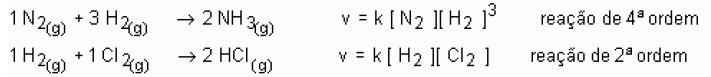Cinética Química
Estuda a velocidade das reações químicas e os fatores que a influenciam e a possibilidade de controlar essa velocidade, tornando-as mais rápidas ou mais lentas. O estudo é feito em reações com velocidade moderada, que pode ser acompanhada, como a decomposição térmica de sais, a combustão de vários compostos orgânicos, a transformação de alimentos pela ação de bactérias.
Teoria das colisões
Partimos do princípio de que as partículas de uma substância química não estão paradas. Elas possuem uma determinada quantidade de energia e se movimentam. Este movimento faz com que se choquem e pode fazer com que ocorra a reação. Para isto, se deve ter quebra de ligações químicas e formação de novas ligações, o que requer colisões eficazes ou efetivas, nas quais são indispensáveis duas condições: colisão suficientemente energética e orientação favorável das moléculas em choque. Segundo a Teoria da Colisões, o que determina a velocidade de reação é a natureza e a quantidade de choques entre as moléculas dos reagentes.
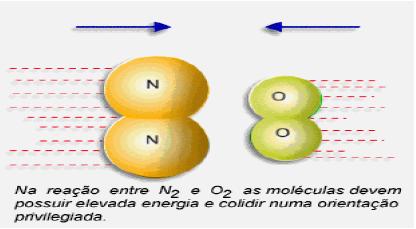
Choques mal orientados, mesmo entre partículas ativadas, não conduzem à reação, assim como choques bem orientados entre partículas não ativadas também não conduzem. Dessa forma, o choque deve ocorrer entre partículas ativadas em uma boa orientação.
Velocidade de reação
A velocidade de consumo de reagentes e formação de produtos é a relação entre a variação de sua quantidade ou de concentração, e o tempo em que ela ocorre.
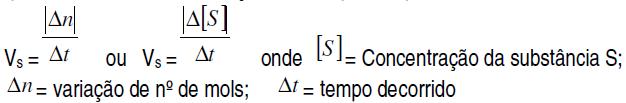
Velocidade média da reação é o módulo da velocidade de consumo de reagentes ou da velocidade de formação de produtos, dividido pelo respectivo coeficiente da substância na equação da reação balanceada.
Dada a equação: 1 N2 (g) + 3 H2 (g) → 2 NH3 (g)
Teremos a equação da velocidade média na reação de formação da amônia:

Fatores que influenciam na velocidade da reação:
A temperatura – O aumento da temperatura faz com que aumente a velocidade da reação. Ex.:Um comprimido efervescente reage amais rápido com água quente do que com a água fria. No refrigerador, a velocidade de decomposição de alimentos por microorganismos é diminuída pela diminuição da temperatura.
A concentração das soluções – o aumento da concentração de um reagente geralmente torna a reação mais rápida.
O estado de divisão de um líquido quando em reação em sistema heterogêneo – uma maior superfície de contato do sólido com o reagente líquido produz maior velocidade de reação. Ex.: O comprimido triturado reage mais rapidamente com a água.
Natureza dos reagentes – Quanto maior o número de ligações a serem rompidas nos reagentes e quanto mais forte forem estas ligações, mais lenta será a reação e vice-versa.
Pressão: Se aumentarmos a pressão (diminuindo o volume, por exemplo), aumentamos o número de colisões e, portanto, a velocidade da reação. Ex.: panela de pressão. Aumentando a pressão, haverá um aumento na temperatura de ebulição da água dentro da panela, possibilitando assim um cozimento mais rápido do alimento imerso.
Presença (concentração e forma física) de um catalisador:
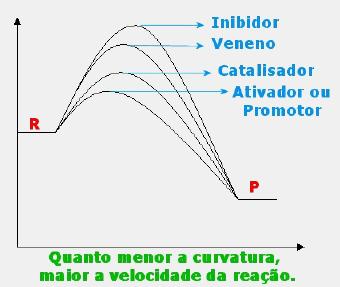
Catalisador: espécie química que acelera a velocidade de uma reação química. Os catalisadores atuam reduzindo a energia de ativação, e por conseqüência, aumentando a velocidade.
Inibidor: espécie química que, juntamente com as moléculas reagentes, faz com que estas reajam a uma velocidade menor. São utilizados como conservantes de alimentos, pois eles retardam a reação de decomposição. Por exemplo, podemos citar na margarina, a ação do conservante EDTA cálcico dissódico.
Ativador espécie química que, juntamente com o catalisador e as moléculas reagentes, faz com que estas reajam a uma velocidade ainda maior do que se estivessem apenas com o catalisador.
Veneno: espécie química que, juntamente com o catalisador e as moléculas reagentes, faz com que estas reajam a uma velocidade menor do que se estivessem apenas com o catalisador.
Energia de ativação
É o valor mínimo de energia que as moléculas dos reagentes devem possuir para que uma colisão entre elas seja eficaz. Quanto maior for a energia de ativação, mais lenta será a reação.
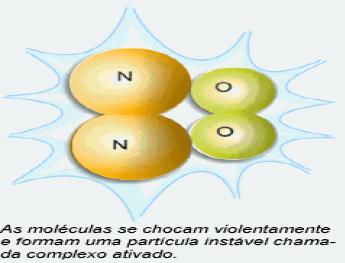
A energia de ativação deve ser entendida como uma dificuldade para ocorrer a reação. Quanto menor a energia de ativação, mais fácil será para a reação acontecer. São reações que necessitam de pouca energia para que ocorram: são reações rápidas.
Quando colisão entre as partículas dos reagentes ocorre com orientação favorável e com energia igual ou superior à energia de ativação, forma-se uma estrutura instável e intermediária entre reagentes e produtos, chamado complexo ativado.
Análise gráfica da energia de ativação
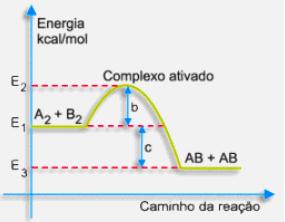

O valor (b) da energia de ativação é maior na endotérmica do que na exotérmica.
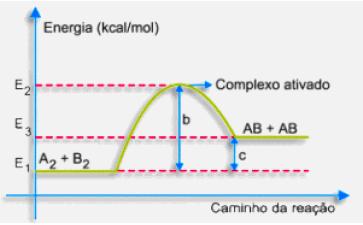

Conclui-se que quanto maior a energia de ativação, menor será a velocidade de reação.
Velocidade instantânea
Para determinar a velocidade instantânea de uma reação, utilizamos uma lei enunciada pelos cientistas noruegueses Maximilian Guldberg e Peter Waage, em 1864, a Lei da ação das massas: “A velocidade de uma reação, em dado instante e a cada temperatura, é proporcional ao produto das concentrações em quantidade de matéria dos reagentes, elevadas a potências iguais aos respectivos coeficientes na equação química balanceada”. Veja:
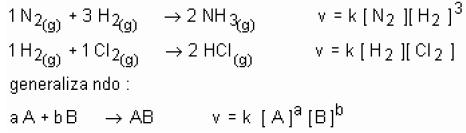
Constante da velocidade é denominada de k. É uma constante de proporcionalidade que relaciona velocidade e concentração. Tem valor constante a uma temperatura e varia com a temperatura. Para dada reação, a constante de velocidade depende fundamentalmente da temperatura, isto é, variando a temperatura, varia o valor de k.
Quando um dos reagentes se encontra no estado sólido, ou líquido em excesso, sua concentração não aparece na equação da Lei da ação das massas:
![]()
Os expoentes a e b na expressão de cálculo da velocidade instantânea, na verdade, são determinados experimentalmente. Existem reações que ocorrem em várias etapas, e a mais lenta determina a velocidade da reação. Por exemplo:
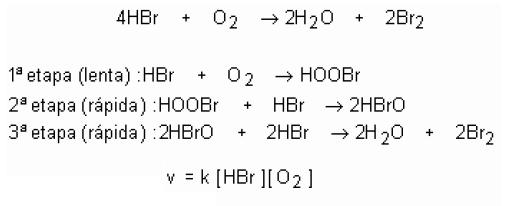
Assim, os expoentes serão iguais aos coeficientes da equação balanceada somente para reações elementares, que ocorrem em uma única etapa.
A ordem de uma reação é dada pela soma dos expoentes aos quais estão elevadas as concentrações na fórmula da velocidade: