Objetivo
Obter cristais de alume de cromo (sulfato duplo de cromo e potássio), [KAl (SO4)2+ 12 H2O] por precipitação.
Material necessário
• dicromato de potássio
• etanol
• ácido sulfúrico concentrado1
• papel de filtro
• vidro de relógio
• balança
• béquer de 200 ml
• proveta de 100 ml
• proveta de 25 ml
• bastão de vidro
• bureta
• termômetro
Procedimento
1) Pese 10 g de dicromato de potássio, com precisão até 0,1 g.
2) Coloque os cristais em um béquer de 200 ml e adicione 75 ml de água quente agitando até dissolução completa do sal.
3) Resfrie a solução e adicione cuidadosamente 8 ml de ácido sulfúrico concentrado.
4) Resfrie a solução.
5) Junte, lentamente, 20 ml de etanol, usando uma bureta e agitando constantemente. Não deixe que a temperatura exceda a 50°C. Se necessário, resfrie com banho de água com gelo.
Esquema de preparo do alume de cromo
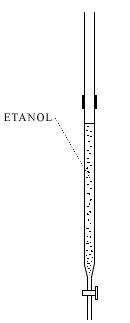
6) Cubra o béquer com um vidro de relógio e deixe a solução em repouso.
7) Após alguns dias, pode-se verificar a formação cristais de cor púrpura.
8) Filtre-os e lave-os com pequenas porções de água.
9) Coloque-os sobre um papel de filtro limpo e deixe secar ao ar.
Comentários
• Alume é o nome comum dado a uma classe importante de compostos, correspondente a sulfatos duplos hidratados de um metal trivalente (alumínio, cromo, ferro) e de um metal alcalino (sódio, potássio), ou de prata.
• Os alumes são facilmente produzidos por precipitação a partir de uma solução que contenha os íons necessários.
O processo de preparação corresponde a uma reação tipo oxido-redução. O dicromato de potássio inicial contém Cr+6 que é reduzido para Cr+3. O etanol é inicialmente oxidado a acetalaldeído, parte do qual se desprende como gás. O restante prossegue sendo oxidado a ácido acético.
• O alume de cromo é apenas ligeiramente solúvel em água e, assim, o volume de água usado para a cristalização deve ser mínimo.
• A solução não deverá ser evaporada e sim mantida abaixo de 65°C a fim de evitar a formação de complexos de sulfato de cromo III.
Por Mabel Rodrigues
