Nos últimos meses, uma notícia muito preocupante tem sido mencionada em manchetes de jornais de todo o mundo: o buraco na camada de ozônio, na região acima da Antártica, ampliou-se de maneira a cobrir a cidade de Punta Arenas, no Sul do Chile, expondo a população a altos níveis de radiação ultravioleta.
Em ocasiões anteriores, as falhas na camada de ozônio no sul do hemisfério apenas atingiam a desabitada Antártica e as águas do Oceano Glacial Antártico.
A NASA avalia que a enorme perfuração equivale a uma área de cerca de 28,3 milhões de Km2, três vezes mais que a área de nosso país!
 |
 |
|---|---|
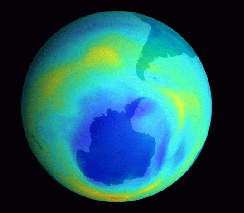
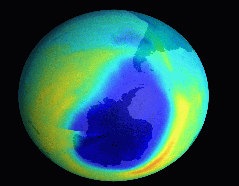
| Fonte: NASA. Buraco de ozônio 28/08/1999. | Fonte: NASA.Buraco de Ozônio 21/09/2000. |
 |
|
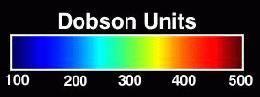
| Fonte: Nasa.Tabela de cores das imagens 1 e 2. |
| Imagens obtidas pelo Espectrômetro da NASA para Mapeamento da Camada Total de Ozônio – um equipamento que encontra-se no satélite “Earth Probe” e revela como o buraco de ozônio (em azul escuro) vem aumentando progressivamente, se estendendo em setembro de 2000 até cobrir o sul do Chile. Nas imagens, a camada de ozônio é medida em termos de unidades Dobson (1 D = 0,01mm de espessura nas CNTP) e representa qual seria sua espessura, se comprimida na atmosfera da Terra. |
A camada de ozônio encontra-se na estratosfera, a uma altura entre quinze a trinta Km acima da superfície da Terra. O ozônio (O3), uma variedade alotrópica do oxigênio, é um gás de cor azulada e odor característico bem forte, bem menos comum que a variedade normal (O2) – moléculas diatômicas de um gás incolor e inodoro – que nós respiramos.
A vida na Terra só se tornou possível devido à imprescindível camada de ozônio, que absorve parte da radiação solar, sobretudo a radiação ultravioleta, altamente prejudicial à saúde podendo causar câncer de pele, catarata, diminuição das defesas imunológicas, afetar plantações e a vida vegetal e animal de um modo geral. A camada de ozônio filtra essa radiação daninha, evitando que ela atinja com toda sua intensidade a superfície de nosso planeta.
Teoricamente, as moléculas de ozônio presentes na estratosfera se formam e se destroém, num processo em equilíbrio. Fatores diversos como as estações, a latitude e as manchas solares contribuem para a variação da concentração de ozônio, e a redução natural que ocorre é sempre seguida de uma recuperação, ciclicamente.
O ozônio se forma quando a radiação ultravioleta da luz do sol atinge a estratosfera, dissociando as moléculas de O2 em oxigênio atômico (O) que rapidamente se recombina com outras moléculas de O2 produzindo O3.
Há cerca de 50 anos, cientistas começaram a observar que o decréscimo na concentração de ozônio já não seguia os ciclos periódicos de perda e ganho, sendo necessário identificar processos recentes que justificassem a queda na concentração de ozônio na sua camada. .
Os fatores que provocam as perdas na camada de ozônio não são simples. Vejamos de uma forma simplificada, como e porque eles atuam: consideremos inicialmente como a atmosfera se comporta acima dos pólos terrestres, particularmente sobre o Polo Sul. Durante o inverno polar não há dias, apenas uma noite contínua, quando a luz do sol não atinge a Terra. Nessas condições um forte vento em torno do pólo se desenvolve entre as camadas médias e as inferiores da estratosfera. Esses ventos, conhecidos como vortex polar, isolam o ar que cobre a região polar. Como não há nenhum aquecimento da luz do sol o ar dentro do vortex polar fica muito frio, possibilitando a formação de nuvens especiais quando a temperatura atinge -80°C. Não são nuvens formadas de gotículas de água, como as que vemos normalmente na atmosfera. Conhecidas como “nuvens estratosféricas polares”, essas nuvens se formam inicialmente como ácido nítrico tri-hidratado, porém à medida que a temperatura continua a diminuir, podem ocorrer grandes gotas de gelo contendo ácido nítrico dissolvido. Veremos mais adiante que é exatamente na superfície dessas nuvens que ocorrem as reações destruidoras do ozônio.

Fonte: Professor Paul Crutzen –
Laureados Prêmio Nobel de Química 1995.
Já em 1970, o Professor Paul Crutzen, do Max Planck Institute for Chemistry, na Alemanha, mostrara que os óxidos de nitrogênio NO e NO2 reagem catalíticamente na camada de ozônio, sem que eles próprios sejam consumidos, daí resultando uma reação em cadeia que acelera a transformação de ozônio em oxigênio:
NO + O3 → NO2 + O2
O3 + luz UV → O2 + O
NO2 + O → NO + O2 com o resultado líquido:
2O3 → 3O2
Em 1974, dois outros cientistas, trabalhando em conjunto – o Professor F. Sherwood Rowland do Departamento de Química da Universidade da Califórnia, em Irvine, e o Professor Mario Molina do Departamento de Química do Massachusetts Institute of Technology (MIT) – publicaram um artigo, na revista Nature, denunciando a ameaça à camada de ozônio dos gases conhecidos como CFC (por conterem cloro, flúor e carbono). Molina e Rowland em uma outra publicação, demonstraram que esses compostos, apesar de quimicamente inertes, eram gradualmente transportados até à camada de ozônio, onde – por efeito da intensa radiação ultravioleta – poderiam se decompor em seus átomos constituintes, liberando cloro atômico, que por sua vez, literalmente “devora” a camada de ozônio.
Em estudos posteriores, efetuados entre 1975 e 1986, Molina e Rowland definiram as reações que conduzem à formação do que ficou conhecido como “reservatórios temporários” para os radicais livres, responsáveis pela destruição do ozônio.
Recentemente, foram demonstradas experimentalmente outras reações químicas onde os compostos “reservatórios” ClONO2 e HCl reagem sobre a superfície das partículas de gelo das nuvens estratosféricas polares fornecendo Cl atômico e ClO. Foi demonstrada ainda, uma seqüência de reações envolvendo a formação e decomposição de ClOOCl, que conduz à destruição catalítica do ozônio, com preservação do cloro atômico que permanece reagindo. Considera-se que essas reações e ciclo catalítico são responsáveis pela maior parte da destruição do ozônio na estratosfera, e cálculos permitem avaliar que um simples átomo de cloro possa eliminar cerca de 100.000 moléculas de ozônio.

Fonte: Mário Molina –
Laureados Prêmio Nobel de Química 1995.
Pelas suas relevantes contribuições à Química os três cientistas em conjunto, Mário Molina, Paul Crutzen e F. Sherwood Rowland receberam o Premio Nobel de Química de 1995.

Fonte: Prof. F. Sherwood Rowland –
Laureados Prêmio Nobel de Química 1995.
Os estudos sobre esse problema extremamente sério prosseguem com a utilização de balões, satélites, estações terrestres – que permitem aquisição de amostras – e estudos in loco, assim como por aplicações de cálculos computacionais sofisticados, como por exemplo, modelagem de reações.
Entretanto, o buraco da camada de ozônio em seu processo cíclico de crescimento e diminuição, no período crítico de setembro e outubro de cada ano, vem se apresentando cada vez maior, apesar das medidas de proteção que vêm sendo tomadas.
“Isto ocorre porque: embora a produção de gases destruidores de ozônio tenha sido controlada por força de acordos internacionais, a concentração desses gases na estratosfera está atingindo seu pico. Devido a sua longa persistência na atmosfera, deveremos esperar muitas décadas até que perfurações na camada de ozônio deixem de ser uma ocorrência anual” afirma o Dr. Michael J. Kurylo, Diretor do Programa de Pesquisas da Atmosfera Superior, da NASA, em Washington, Estados Unidos.
