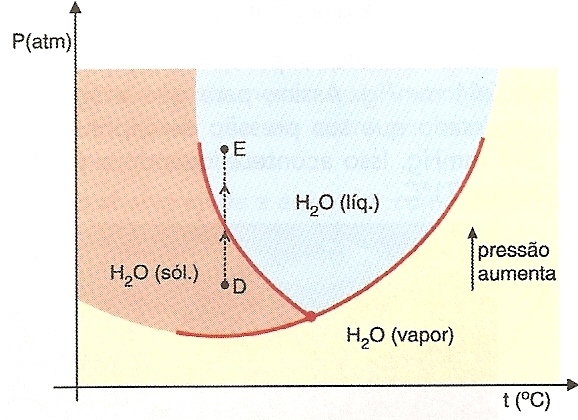
Corresponde a um gráfico que nos fornece importantes informações sobre o equilíbrio entre as fases sólido-líquido, sólido-vapor e líquido – vapor de uma substância pura.
O diagrama abaixo é um diagrama de fases para a água pura e foi obtido a uma pressão constante de 760 mmHg.
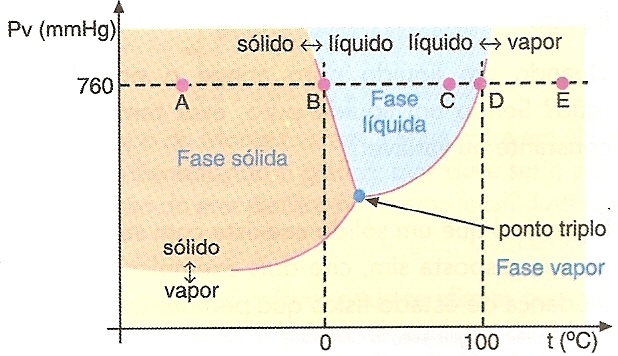
A seguir, na linha de pressão constante (760 mmHg), serão analisadas as temperaturas representadas pelos pontos A, B, C, D e E.
►Na temperatura representada pelo ponto C, a água se encontra unicamente no estado líquido.
►Diminuindo a temperatura do ponto C até o ponto B, o líquido começa a congelar. A temperatura representada pelo ponto B é a temperatura de congelamento da água pura sob pressão de 760 mmHg seu valor corresponde a 0ºC.
►Na temperatura representada pelo ponto A, a água se encontra unicamente no estado sólido.
►Aumentando-se a temperatura do ponto C até o ponto D, o líquido começa ferver. A temperatura representada pelo ponto D é a temperatura de ebulição da água pura e, sob pressão de 760 mmHg, seu valor corresponde a 100ºC.
►Aumentando a temperatura do ponto D até o ponto E, toda água líquida é convertida em vapor.
►Na temperatura representada pelo ponto E, a água se encontra unicamente no estado de vapor.
O ponto triplo representa a combinação pressão – temperatura no qual as três fases da substância (no caso a água) – sólida, líquida e vapor – coexistem em equilíbrio e que se encontram a 4,579 mmHg de pressão e 0,0098ºC de temperatura.
Para ilustrar, vejamos o que ocorre com a “patinação no gelo”.
Os patins têm apoios, as lâminas, muito finas, o que faz com que uma pessoa com 60 Kg exerça uma pressão no gelo equivalente a 500 atm.
Lembre-se que:
Pressão = Força / área
Devido a essa grande pressão, o gelo abaixo das lâminas sobre fusão (ver trecho DE no gráfico), formando uma fina camada de água líquida que atua como lubrificante entre os patins e o gelo.
Após a passagem das lâminas, a água volta à pressão inicial, ocorrendo o regelo.