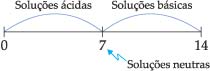
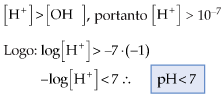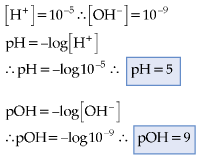| Em 1909, o químico dinamarquês Sörensen propôs as definições: pH = – log [H+] pOH = – log [OH-] Portanto, podemos fazer as seguintes relações, a 25ºC: · Produto Iônico da Água [H+] . [OH-] = 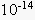 → pH + pOH = 14 → pH + pOH = 14· Meio Neutro [H+] = [OH-] = 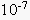 → pH = pOH = 7 → pH = pOH = 7· Meio Ácido [H+] > 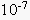 → pH < 7 [OH-] < → pH < 7 [OH-] < 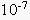 → pOH > 7 → pOH > 7· Meio Básico [H+] < 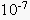 → pH > 7 [OH-] > → pH > 7 [OH-] > 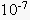 → pOH < 7 → pOH < 7Podemos representar graficamente a escala de pH e pOH: |
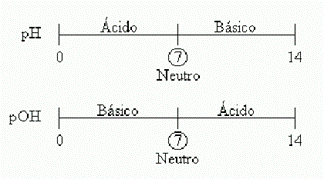
| pH e pOH |
Para não se trabalhar com potências negativas, como, por exemplo, 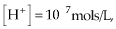 Peter L. Sörensen propôs uma nova escala para as medidas de acidez e basicidade das soluções, utilizando logaritmo segundo as definições: Peter L. Sörensen propôs uma nova escala para as medidas de acidez e basicidade das soluções, utilizando logaritmo segundo as definições: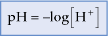
1. Para soluções ácidas |
2. Para soluções básicas
![]()
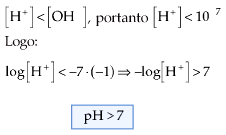
![]()
Exemplo
![]()
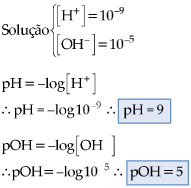
3. Para soluções neutras
![]()
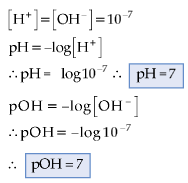
![]()
Portanto, a 25°C:
O pH de soluções de sais
Quando um sal se dissolve na água, o pH resultante pode ser básico, ácido ou neutro, dependendo da natureza do sal:
- Se for um sal de ácido forte e base forte, o pH é próximo de 7 (neutro), e nenhum dos íons hidrolisam. Ex: NaCl, K2SO4.
- Se for um sal de ácido fraco e base forte, a solução é básica (pH > 7), pois somente o ânion hidrolisa, aumentando a concentração de íons OH-. Ex: NaF, K(CH3COO).
- Se for um sal de ácido forte e base fraca, a solução é ácida (pH < 7), pois somente o cátion hidrolisa, aumentando a concentração de íons H3O+. Ex: NH4Cl, Al2(SO4)3.
- No caso de um sal de ácido e base fracos, ambos os íons sofrerão hidrólise. Para se determinar o pH da solução, precisaremos conhecer os valores de Kh para o ânion e para o cátion. Se o Kh para hidrólise do cátion (que tende a tornar a solução ácida) for maior do que o Kh para hidrólise do ânion (que tende a tornar a solução básica), a solução será ácida, por causa de um pequeno excesso de íons H3O+. E vice-versa.
Comentários