Reação Irreversível (→)
É aquela que se processa em um sentido até o consumo total dos reagentes.
Exemplos:
Combustão do palito de fósforo, formação da ferrugem, neutralização da acidez estomacal.
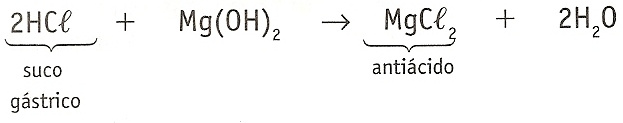
Reação Reversível (⇔)
É aquela que se processa no sentido direto (reagentes → produtos) e no sentido inverso (produtos → reagentes), até atingir um estágio de equilíbrio químico.
.jpg)
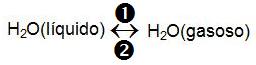
Quando v1 = v2, temos o equilíbrio químico.
Equilíbrio Químico
Estágio de equilíbrio dinâmico em que as velocidades das reações direta e inversa são iguais.
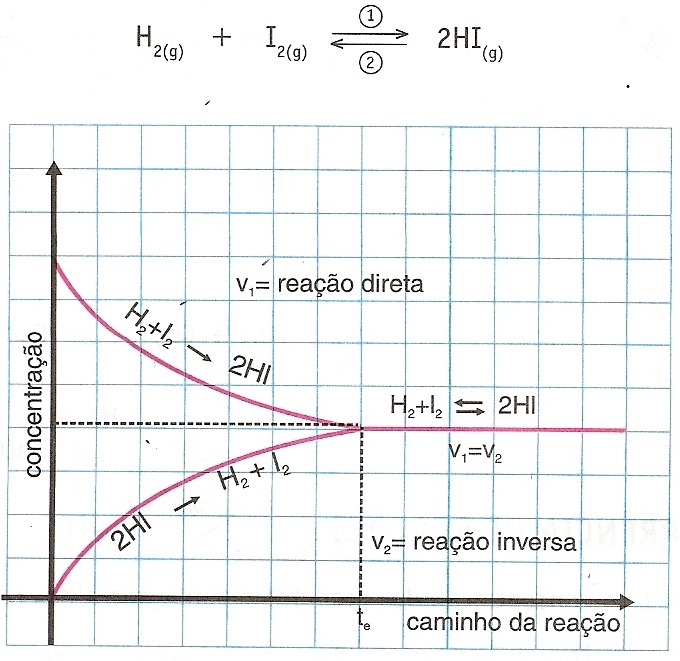
Constante de Equilíbrio (Kc)
É obtida matematicamente isolando-se as constantes cinéticas das equações das velocidades das reações direta e inversa.
aA + bB ⇔ cC + dD
v1 = k1[A]a.[B]b e v2 = k2[C]c.[D]d, no equilíbrio, v1 = v2 ⇒ k1[A]a.[B]b = k2[C]c.[D]d
isolando o k1 e k2, temos:
.jpg)
Como o quociente de duas constantes é outra constante, temos:
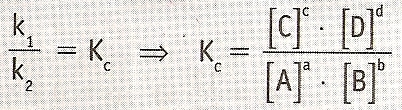
kc é a constante de equilíbrio em termos das concentrações molares (mol/L). Lembre-se que: [ ] = mol/L.
Observação:
• Kc não varia com a concentração nem com a pressão, mas varia com a temperatura.
• Quanto maior o Kc, maiores são as concentrações dos produtos em relação às dos reagentes, no equilíbrio.
• Quanto menor o Kc, menores são as concentrações dos produtos em relação às dos reagentes, no equilíbrio.
• Após atingir o equilíbrio, as concentrações de todos os participantes ficam constantes, porém não necessariamente iguais.
• O equilíbrio é dito dinêmico, pois no nível MACROSCÓPICO a reação aparenta está cessada, mas no nível microscópico ela continua ininterruptamente.
Exemplos de escrita de kc:
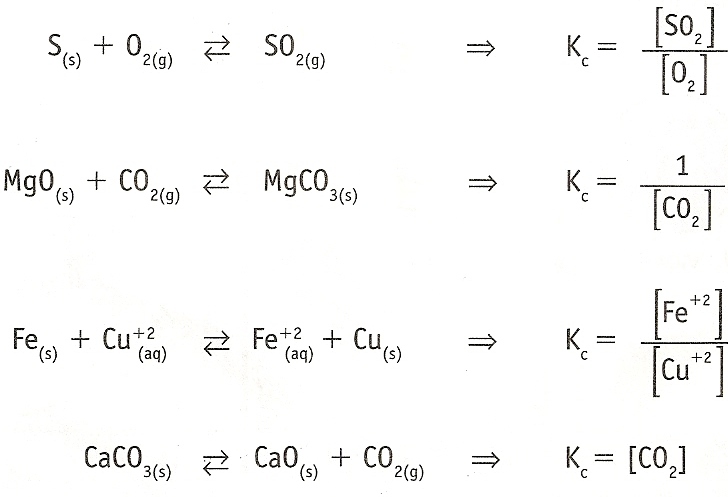
Ocorrência das reações
kc> 1 ⇒ concentração dos produtos é maior que a dos reagentes, logo a reação direta prevalece sobre a inversa.
kc> ⇒ concentração dos reagentes é maior que a dos produtos, logo a reação inversa prevalece sobre a direta.
Grau de equilíbrio (![]() )
)

Constante de equilíbrio em termos das pressões parciais de gases (kp)
.jpg)
em que p(A), p(B), p(C) e p(D) são as ppressões parciais dos gases A, B, C e D.
Observação:
1.Na expressão de kp devem ser usados apenas os componentes gasosos.
2. Na expressão do kc os componentes sólidos e líquidos puros não são usados.
3. Tanto kp e kc variam apenas com a temperatura.
Relação entre kp e kc
aA + bB ⇔ cC + dD
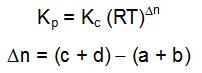
Equilíbrios heterogêneos – quando existir mais de um estado físico entre os participantes.
