Sabemos que o indicador fenolftaleína adquire cor rosa em uma solução de soda cáustica. Entretanto, se gotejarmos uma solução de ácido muriático até que a mistura fique ácida, o indicador torna-se incolor. Mas a solução ficará rosada novamente se adicionarmos uma solução de soda cáustica em quantidade suficiente.
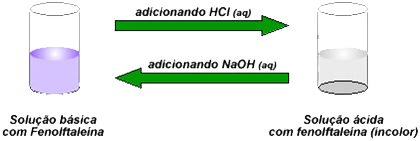
Essa simples experiência mostra um fato curioso e de extrema importância: os equilíbrios podem ser “empurrados” (deslocados) para um ou outro sentido.
Deslocamentos de equilíbrios químicos são fundamentais em muitos processos biológicos, tais como a manutenção da acidez do sangue, em processos respiratórios e na absorção de nutrientes e de medicamentos.
Um modelo simples
Para uma primeira idéia sobre deslocamentos de equilíbrio, considere um equilíbrio do tipo A <—> B, com 6 moléculas de cada participante.
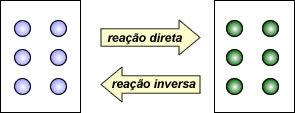
Equilíbrio I. Seis moléculas de cada substância, transformando-se com velocidades iguais (v1 = v2).
Admitindo que o número total de moléculas permaneça constante, há diversas maneiras de se atingir um novo equilíbrio, com maior número de moléculas A ou B.
Se o e equilíbrio for empurrado para a direita, o novo equilíbrio terá maior número de moléculas B, enquanto necessariamente diminuirá a quantidade de moléculas de A.
Dizemos, então, que o equilíbrio foi deslocado para a direita.
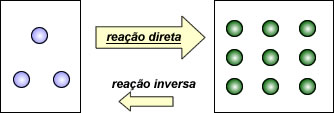
Equilíbrio II. Deslocamento para a direita. A reação direita é favorável.
Quando forem realizadas alterações que favoreçam a reação inversa, diremos que o equilíbrio foi deslocado para esquerda.
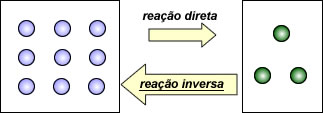
Equilíbrio III. Deslocamento para a esquerda. A reação inversa é favorecida.
Comentários
Em algumas situações, os químicos costumam indicar deslocamentos de equilíbrios utilizando setas com tamanhos diferentes. Mas isso não quer dizer que as velocidades dos processos opostos sejam diferentes.
Lembre que, em qualquer situação de equilíbrio, não importando em que sentido ele esteja deslocado, as velocidades dos processos opostos serão sempre iguais.
Mantendo-se a temperatura constante, os deslocamentos não afetam a constante de equilíbrio.
Para a direita ou para a esquerda ?
Um equilíbrio não se desloca por vontade própria. O que deve ocorrer, na verdade, são alterações externas que forçarão o deslocamento para um dos lados.
Em 1888, Lê Chatelier enunciou um princípio que nos nos permite prever em que sentido o equilíbrio será deslocado.

Alterando concentrações, retirando um participante, a influência da temperatura, alterando a pressão e a ação do catalisador
Aumento da concentração → Deslocamento do equilíbrio no sentido da reação em que a substância adicionada é consumida.
Diminuição da concentração → Deslocamento de equilíbrio no sentido da reação em que a substância retirada é produzida.
Aumento de temperatura → Deslocamento de equilíbrio no sentido da reação em que o calor é absorvido (endotérmico).
Redução de temperatura → Deslocamento de equilíbrio no sentido da reação em que o calor é reposto (exotérmico).
Aumento de Pressão → Desloca o equilíbrio no sentido do menor volume (somente para gases).
Diminuição de Pressão → Desloca o equilíbrio no sentido do maior volume (somente para gases).
DICA: Menor volume ou Maior volume, a gente analisa pelo número de mols em uma dada reação. Se aumentarmos a pressão em uma reação 1:1:2, ele deslocará para onde tem menor volume, ou seja, para esquerda na reação inversa.
EXEMPLO:
![]()
Aumentando a temperatura → desloca para esquerda.
Aumentando a pressão → desloca para a direita. Pois temos uma reação 1:3:2, com aumento de pressão, teremos um deslocamento para onde tem maior volume, ou seja, para esquerda.
Aumentando a concentração de N2 → desloca para direita.
Diminuindo a concentração de N2 → desloca para esquerda.
Catalisador
Sabemos que o catalisador diminui a energia de ativação de uma reação.
No caso dos equilíbrios, o catalisador diminui igualmente as energias de ativação nos dois sentidos. Com isso, ele aumenta a velocidade da reação direta e também da reação inversa.
Podemos concluir, portando, que o catalisador não afeta um equilíbrio.
