Materiais e reagentes
• Sete tubos de ensaio (ou outros recipientes estreitos de vidro transparente)
• Dois béqueres (ou copos de vidro transparentes)
• Uma seringa de plástico
• Um conta-gotas
• Oito pregos de ferro
• Dois pedaços de fio de cobre (bem finos)
• Dois pedaços de magnésio (ou zinco)
• Cloreto de sódio – NaCl – (sal de cozinha)
• Suco de limão
Procedimento
• Em um béquer, misture 20mL de água e uma colher de chá de sal. Agite a mistura até a completa dissolução do sal. Vamos chamar essa solução de A.
• No outro béquer, misture 10mL de suco de limão e 10mL de água. Chamaremos essa solução de B.
• Prepare os tubos de ensaio conforme a tabela a seguir:
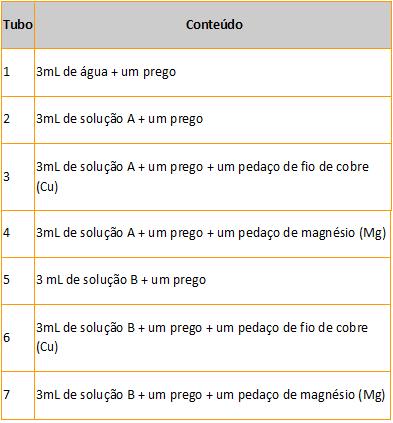
Essas soluções representam diferentes ambientes em que o Ferro (Fe) pode ser encontrado: úmido, salino devido à presença de água do mar, ácido por causa da chuva ou em presença de outros metais.
O que você observou nos tubos logo que os preparou?
Anote suas observações. Deixe os tubos em repouso por dois dias aproximadamente.

Discussão final
• Como estava o aspecto do prego em cada um dos tubos ao final da experiência?
• Há diferenças no aspecto do ferro nos diversos meios analisados? Quais?
• Houve reação em todos os tubos? Em quais? Você poderia explicar esse fato?
• Que tipo de reação química o ferro sofreu?
• O fio de cobre sofreu alguma modificação? Qual?
• E o pedaço de magnésio?
• Será que conseguiremos criar uma situação em que o ferro não sofra corrosão? Por que isso poderá ocorrer ?
• Você consegue imaginar uma aplicação prática para esse fenômeno?
Os cascos de navios costumam ter placas de zinco presas na superfície em contato com a água do mar.
Existe alguma relação entre a experiência e esse fato?
Fonte: http://www.educacaopublica.rj.gov.br
