Antes de iniciarmos o conceito de hidrólise salina, é extremamente importante a revisão sobre a força de ácidos e bases, tendo em vista a dependência direta desse assunto com a hidrólise.
Revisando a força de ácidos e bases:
ÁCIDOS:
a) Força para hidrácidos (ácidos que não contém oxigênio):
Fortes: HCl , HBr, HI.
Moderado: HF
Fracos: HCN e H2S.
Note que os hidrácidos da família 17 (7A) são fortes, mas quanto maior a eletronegatividade do halogênio, menor a força do hidrácido correspondente, por isto o HF é moderado, embora o flúor seja halogênio. No entanto, diante de problemas de hidrólise, deve-se considerar o HF com sendoFORTE, pois sua constante de acidez (Ka) = 3,5.10-4 (valores de Ka da ordem de 10-5 ou menor correspondem a ácidos fracos).
b) Força para oxiácidos (ácidos que contêm oxigênio em sua estrutura):

BASES:
Força de Bases ou Hidróxidos:
BASES FORTES: FAMÍLIA 1A (todos) e 2A (exceto Be(OH)2 e Mg(OH)2
FAMÍLIA 1A = Li Na K Rb Cs Fr
NaOH, KOH, LiOH, Ca(OH)2, Ba(OH)2, Ba(OH)2, ETC.
BASES FRACAS: Todas as DEMAIS (incluindo o Be(OH)2 e Mg(OH)2, as bases de metal de transição, etc).
AgOH, NH4OH, Fe(OH)2, Fe(OH)3, Al(OH)3, ETC.

Conceito de HIDRÓLISE: é a “quebra” de um sal pela água, ou seja a reação deste com a água, é o processo inverso a uma reação de neutralização.
SAL + ÁGUA ⇔ BASE + ÁCIDO
Lembre-se:
► o cátion (espécie positiva) sempre pertencerá a base. Ex. NaOH → cátion Na+
► o ânion (espécie negativa) sempre pertencerá ao ácido. Ex. HCl → Cl–
Existem quatro casos envolvendo a hidrólise de sais:
1º CASO – HIDRÓLISE DE SAL DE BASE FRACA E ÁCIDO FORTE
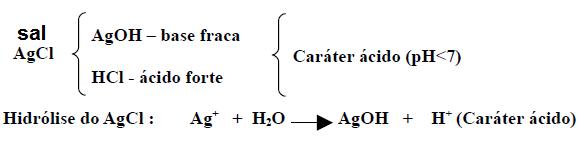
.jpg)
2º CASO – HIDRÓLISE DE SAL DE BASE FORTE E ÁCIDO FRACO:
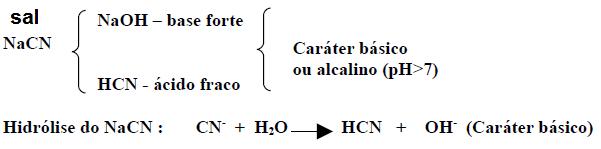
.jpg)
3º CASO – HIDRÓLISE DE SAL DE BASE FRACA E ÁCIDO FRACO:
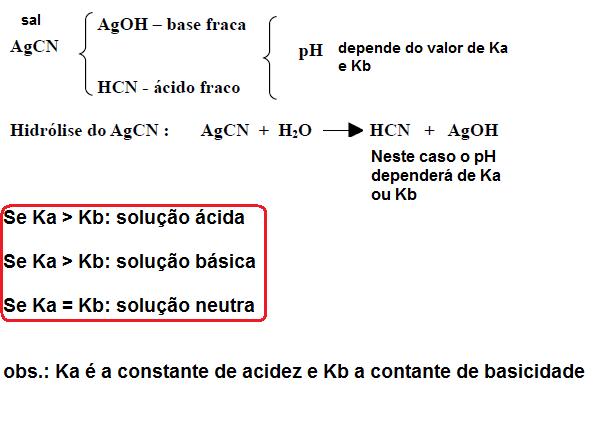
.jpg)
4º CASO – HIDRÓLISE DE SAL DE BASE FRACA E ÁCIDO FRACO:
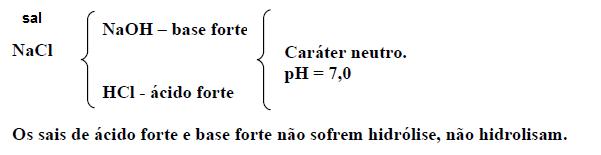
.jpg)
Logo, os casos de hidrólise são fixados nos seguintes casos (resumo):

De uma maneira geral, temos sempre que considerar a seguinte informação:
.jpg)
Aplicação do conteúdo ao cotidiano:
Hidrólise Salina e Solo
pH do solo depende de sua composição. Terrenos pantanosos têm pH por volta de 3,5, devido à presença de grande quantidade de ácidos provenientes do húmus
Terrenos sedimentares, formados por sílica (SiO2), devido à formação em pequena quantidade de acido silícico (H4SiO4), apresentam pH próximo de 6,0. Terrenos de origem vulcânica, ricos em silicatos de cálcio e magnésio, devido à sua hidrólise, apresentam pH superior a 7.

![]()
SiO4-4 + 4 HOH H4SiO4 + 4 OH-
Regiões de solo calcário (carbonatos de cálcio, magnésio etc.) já apresentam pH muito maior, por volta de 9. Para corrigir a acidez dos solos, podemos adicionar CaO:
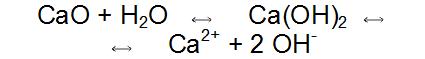
É muito mais barato, no entanto, adicionarmos CaCO3, o qual, por hidrólise ácida, também produz Ca(OH)2 . Cada tipo de planta cresce melhor em solos que possuem uma faixa específica de pH; fora dessa faixa, elas não se desenvolvem bem nem produzem a quantidade esperada de flores e frutos.
A tabela a seguir apresenta exemplos de faixa de “pH ótimo” para algumas plantas:

