LIGAÇÃO s : é a ligação formada pela interpenetração frontal de orbitais (segundo um mesmo eixo). A ligação s é forte e difícil de ser rompida. Pode ser feita com qualquer tipo de orbital atômico;
LIGAÇÃO p : é a ligação formada pela aproximação lateral de orbitais (segundo eixos paralelos). A ligação p é mais fraca e mais fácil de ser rompida; Só ocorre entre orbitais atômicos do tipo “p”;
Obs.: Quando dois átomos estabelecem uma dupla ou tripla ligação, a primeira é sempre do tipo s, a Segunda e a terceira ligação, se houver, serão obrigatoriamente do tipo p .
Obs.: Os orbitais atômicos se unem para formar orbitais moleculares.

HIBRIDAÇÃO
| Família |
Hibridação |
Geometria |
Angulo(s) |
Exemplo |
|
2A |
Sp |
Linear |
180° |
BeH2 (C2H2*) |
|
3A |
Sp2 |
Trigonal plana |
120° |
BH3 (C2H4*) |
|
4A |
Sp3 |
Tetraédrica |
109°28′ |
CH4* |
|
5A |
Sp3d |
Bipirâmide trigonal |
90° e 120° |
PCl5 |
|
6A |
Sp3d2 |
Octaédrica |
90° |
SF6 |
Obs.: Carbono: (CH4*) = 4 ligações simples: sp3; (C2H4*) = 01 dupla e 02 simples: sp2; (C2H2*) = 02 duplas ou 01 tripla e 01 simples: sp)
Obs.: Hibridação da amônia (NH3) e da água (H2O): sp3;
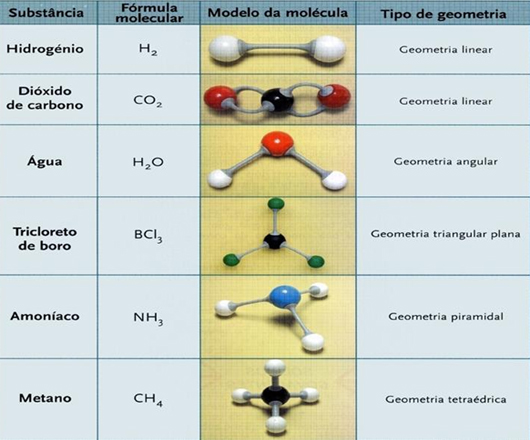
GEOMETRIA MOLECULAR
| N.º de átomos | Existe(m) pare(s) de elétrons livres no átomo central | Geometria – ângulo | Exemplos | Polaridade |
| 02 | ———————– | Linear – 180° | HCl; H2; CO | Polar ou Apolar |
| 03 | Não | Linear – 180° | CO2; HCN; N2O | Polar ou Apolar |
| 03 | Sim | Angular – variável | H2O; SO2; H2S | Polar |
| 04 | Não | Trigonal plana – 120° | BF3; SO3; CH2O* | Apolar (*polar) |
| 04 | Sim | Piramidal – variável | NH3; PH3; SOCl2 | Polar |
| 05 | ———————– | Tetraédrica – 109°28′ | CH4;SiCl4; POCl3 | Polar ou Apolar |
| 06 | ———————– | Bipirâmide trigonal – 90° e 120° | PCl5 | Apolar |
| 07 | ———————– | Octaédrica – 90° | SF6 | Apolar |