NÚMERO DE OXIDAÇÃO (Nox)
É o número que mede a carga real (em compostos iônicos) ou aparente (em compostos covalentes) de uma espécie química.
Exemplos:
No “NaCl“ o átomo de sódio cedeu 1 elétron para o átomo de cloro. Então:
. O sódio origina o íon sódio (Na1+).
e
. O cloro origina o íon cloreto ( Cl –1).
A carga do íon sódio é o número de oxidação do sódio neste composto.
Nox = + 1
A carga do íon cloreto é o número de oxidação do cloro neste composto.
Nox = – 1
Em compostos covalentes o número de oxidação negativo é atribuído ao elemento mais eletronegativo e o número de oxidação positivo ao elemento menos eletronegativo.
Exemplo:
H – Cl
O cloro é mais eletronegativo que o hidrogênio, então:
O cloro atrai para si um elétron, então o seu Nox será – 1, e o hidrogênio tem o seu elétron afastado, então o seu Nox será + 1.
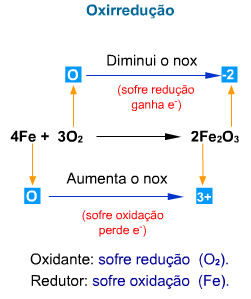
Podemos associar os conceitos de oxidação e redução ao de número de oxidação.
Oxidação é a perda de elétrons ou o aumento do número de oxidação (Nox).
Redução é o ganho de elétrons ou a diminuição do número de oxidação (Nox).
A espécie química que provoca a redução de um elemento chama-se agente redutor e, a espécie química que provoca a oxidação de um elemento chama-se agente oxidante.
REGRAS PRÁTICAS PARA DETERMINAR O Nox
1ª regra:
Todo elemento em uma substância simples tem Nox igual a zero.
Exemplos:
O2: Nox de cada átomo de oxigênio é zero.
N2: Nox de cada átomo de nitrogênio é zero.
Ag: Nox do átomo de prata é zero.
2ª regra:
O Nox de alguns elementos em substâncias compostas é constante.
O hidrogênio tem Nox igual a + 1.
Os metais alcalinos têm Nox igual a + 1.
Os metais alcalinos terrosos têm Nox igual a + 2.
O oxigênio tem Nox igual a – 2.
Os halogênios em halogenetos têm Nox igual –1.
A prata (Ag) tem Nox igual a + 1.
O zinco (Zn) tem Nox igual a + 2.
O alumínio (Al) tem Nox igual a + 3.
O enxofre (S) em sulfetos tem Nox igual a – 2.
Exemplos:
NaCl
- O sódio tem Nox = + 1
- O cloro tem Nox = – 1
Ca(OH)2
. O cálcio tem Nox = + 2.
. O hidrogênio tem Nox = +1.
. O oxigênio tem Nox = – 2.
H2S
. O hidrogênio tem Nox = + 1.
. O enxofre tem Nox = – 2.
Casos particulares importantes
Nos hidretos metálicos o “hidrogênio” possui Nox igual a – 1.
Nos peróxidos o “oxigênio” possui Nox igual a – 1.
Exemplos:
H2O2
Este composto é um peróxido
. O hidrogênio tem Nox = +1.
. O oxigênio tem Nox = – 1.
NaH
Este composto é um hidreto metálico
. O sódio tem Nox = +1.
. O hidrogênio tem Nox = – 1.
3ª regra:
A soma algébrica dos Nox de todos os átomos em uma espécie química neutra é igual a zero.
Exemplo:
NaOH
. O Nox do sódio é + 1.
. O Nox do oxigênio é – 2.
. O Nox do hidrogênio é + 1.
Calculando a soma algébrica, teremos:
(+ 1) + ( – 2) + ( + 1) = 0
Esta regra possibilita a cálculo do Nox de um elemento químico que não possui Nox constante.
Exemplo:
CO2
. O Nox do carbono é desconhecido ( x ).
. O Nox de cada átomo de oxigênio é – 2.
Então:
x + 2 . ( – 2 ) = 0
x – 4 = 0
x = + 4
Portanto o Nox do átomo de carbono neste composto é igual a + 4.
4ª regra:
A soma algébrica dos Nox de todos os átomos em um íon é igual à carga do íon.
Exemplo:
NH4+1
. O átomo de nitrogênio não tem Nox constante ( x ).
. Cada átomo de hidrogênio possui Nox igual a + 1.
. O íon tem carga + 1.
Calculando a soma algébrica, teremos:
x + 4 . ( + 1 ) = + 1
x + 4 = 1
x = 1 – 4
x = – 3
Então o Nox do átomo de nitrogênio é igual a – 3.
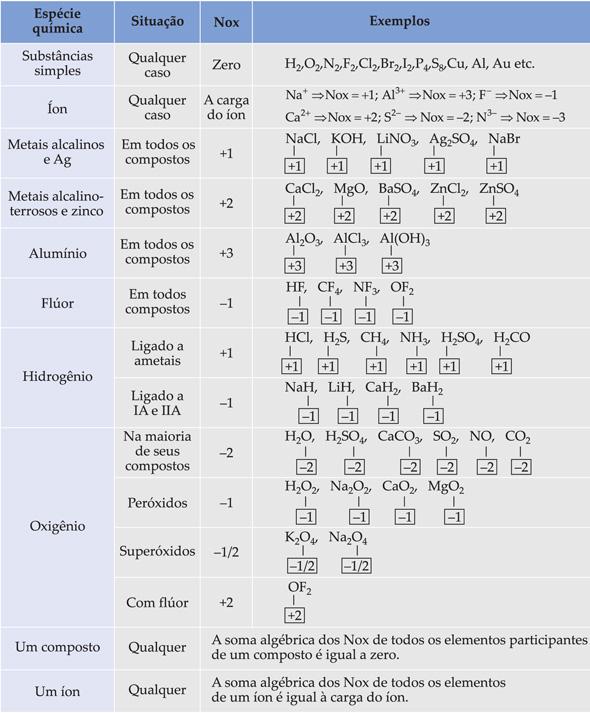
Resumo Geral tabelado:
Noção sobre reação de oxirredução:
Exercícios:
1. (MACKENZIE-SP) sabendo que o cloro pertence à família dos halogênios, a substância na qual o cloro apresenta número de oxidação máximo é:
a) Cl2O5.
b) HCl.
c) Cl2O.
d) HClO4.
e) Cl2.
2. Considere os compostos de fórmulas:
NaNO2; H2PO3; Ba2As2O7
Os Nox dos elementos que pertencem ao grupo 15, presentes nesses compostos, são, respectivamente:
a) + 1 + 1 e + 2.
b) + 2, – 4 e – 5.
c) + 3, – 2 e – 5.
d) + 3 + 1 e + 3.
e) + 3 + 4 e + 5.
3. Os números de oxidação do enxofre nas espécies SO2 e SO42- são, respectivamente:
a) zero e + 4.
b) + 1 e – 4.
c) + 2 e + 8.
d) + 4 e + 6.
e) – 4 e – 8.
4. Descobertas recentes da medicina indicam a eficiência do óxido nítrico, NO, no tratamento de determinado tipo de pneumonia. Sendo facilmente oxidado a NO2, quando preparado em laboratório, o ácido nítrico deve ser recolhido em meio que não contenha oxigênio. Os Nox do nitrogênio no NO e NO2 são, respectivamente:
a) + 3 e + 6.
b) + 2 e + 4.
c) + 2 e + 2.
d) zero e + 4.
e) zero e + 2.
5. Assinale a alternativa cuja equação química não representa uma reação de oxi-redução:
a) N2 + H2 → 2NH3.
b) Cl2 + NaI → NaCl + I2.
c) Fe + HCl → FeCl2 + H2.
d) C2H6O + O2 → CO2 + H2O.
e) Na2O + HCl → NaCl + H2O.
6. Na equação representativa de uma reação de oxi-redução:
Ni + Cu 2+ → Ni2+ + Cu
a) O íon Cu2+ é o oxidante porque ele é oxidado.
b) O íon Cu2+ é o redutor porque ele é reduzido.
c) O Ni é redutor porque ele é oxidado.
d) O Ni é o oxidante porque ele é oxidado.
e) O Ni é o oxidante e o íon Cu2+ é o redutor.
7. Na reação de oxi-redução H2S + I2 → S + 2HI, as variações dos números de oxidação do enxofre e do iodo são, respectivamente:
a) +2 para zero e zero para +1.
b) zero para +2 e +1 para zero.
c) zero para -2 e -1 para zero.
d) zero para -1 e -1 para zero.
e) –2 para zero e zero para -1.
8. Para uma reação de óxido-redução:
a) o agente redutor sofre redução.
b) a substância que perde o elétron é o agente redutor.
c) o número de oxidação do agente oxidante aumenta.
d) o número de oxidação do agente redutor diminui.
e) a substância que perde elétron é o agente oxidante.
9. O elemento X reage com o elemento Z, conforme o processo:
Z3– + X → Z1– + X2–
Nesse processo:
a) Z ganha elétrons de X.
b) X ganha elétrons de Z.
c) X e Z cedem elétrons.
d) X e Z perdem elétrons.
e) X e Z cedem e ganham elétrons, respectivamente.
10. Tratando-se o fósforo branco (P4) com solução aquosa de ácido nítrico (HNO3) obtêm-se ácido fosfórico e monóxido de nitrogênio, segundo a equação química equilibrada.
3 P4 + 20 HNO3 + 8 H2O → 12 H3PO4 + 20 NO
Os agentes oxidante e redutor dessa reação são, respectivamente:
a) P4 e HNO3.
b) P4 e H2O.
c) HNO3 e P4.
d) H2O e HNO3.
e) H2O e P4.
11. O ferro galvanizado apresenta-se revestido por uma camada de zinco. Se um objeto desse material for riscado, o ferro ficará exposto às condições do meio ambiente e poderá formar o hidróxido ferroso. Nesse caso, o zinco, por ser mais reativo, regenera o ferro, conforme a reação representada abaixo:
Fe(OH)2 + Zn → Zn(OH)2 + Fe
Sobre essa reação pode-se afirmar:
a) O ferro sofre oxidação, pois perderá elétrons.
b) O zinco sofre oxidação, pois perderá elétrons.
c) O ferro sofre redução, pois perderá elétrons.
d) O zinco sofre redução, pois ganhará elétrons.
e) O ferro sofre oxidação, pois ganhará elétrons.
12. Na reação representada pela equação abaixo, concluímos que todas as afirmações estão corretas, exceto:
2 Na + 2 H2O → 2 NaOH + H2
a) O sódio é o agente redutor.
b) O íon hidroxila é reduzido.
c) O sódio é oxidado.
d) A água é o agente oxidante.
e) O hidrogênio é reduzido.
13. Em uma reação de oxi-redução, o agente oxidante:
a) perde elétrons.
b) sofre oxidação.
c) aumenta sua carga positiva.
d) sofre redução.
e) passa a ter carga nula.
14. O processo em que um átomo cede elétron a outro é denominado transformação de oxidoredução, que pode ser identificada na situação seguinte:
a) Envelhecimento do ouro.
b) Formação de ferrugem.
c) Conservação de alimentos.
d) Dissolução de comprimidos efervescentes.
e) Reação de neutralização entre um ácido e uma base de Arrhenius.
Gabarito:
1.(D); 2.(E); 3.(D); 4.(B); 5.(E); 6.(C); 7.(E); 8.(B); 9.(B); 10.(C); 11.(B); 12.(B); 13.(D); 14.(B).
