Uma das razões pelas quais as propriedades de um sistema em equilíbrio são muito importantes é que todas as reações tendem a alcançar um equilíbrio. De fato, se permitirmos, todas as reações químicas atingem um estado de equilíbrio, embora isso nem sempre seja evidente. Às vezes dizemos que uma reação química foi “completada”, mas rigorosamente falando, não existem reações que consumam 100% dos reagentes. Todos os sistemas que reagem alcançam um estado de equilíbrio, no qual permanecem pequenas quantidades de reagentes que estão sendo consumidos, até que seja quase impossível de se medir.
Considere a seguinte reação: CO2 (g) + H2 (g) ![]() CO(g) + H2O(g)
CO(g) + H2O(g)
Suponha que certa quantidade de CO2 e H2 estão contidas em um recipiente hermeticamente fechado e que disponhamos de um instrumento que nos permita acompanhar o desenvolvimento da reação. Após o início da reação, percebemos que as concentrações dos reagentes (CO2 e H2) diminuem e que as dos produtos (CO e H2O) aumentam. (Todas essas concentrações aumentam e diminuem na mesma proporção, já que a relação estequiométrica de todas as substâncias envolvidas, em razão mol por mol, é de 1:1). Veja abaixo o gráfico que representaria esse equilíbrio químico:
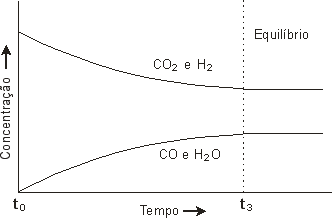
Considerando que a reação se inicia no instante t0, as concentrações dos reagentes diminuíram e as dos produtos aumentaram. Veja, pelo gráfico, que as variações de concentração vão se tornando menos acentuadas desde o início da reação até o instante t3, em que o equilíbrio foi atingido. Isso significa que as velocidades de troca se tornam menores com o passar do tempo. No tempo t0 somente pode ocorrer a reação no sentido da formação dos produtos: A + B ![]() C + D (reação direta). Entretanto, após certo tempo, quando significativa quantidade de produto já foi formada, pode se iniciar a reação no sentido contrário, ou seja, de se regenerar os reagentes: C + D
C + D (reação direta). Entretanto, após certo tempo, quando significativa quantidade de produto já foi formada, pode se iniciar a reação no sentido contrário, ou seja, de se regenerar os reagentes: C + D ![]() A + B (reação inversa). A velocidade da reação direta diminui com o tempo, devido ao decréscimo de reagentes (menor número de choques efetivos). Ao mesmo tempo, a velocidade da reação inversa aumenta, por causa do aumento da concentração dos produtos.
A + B (reação inversa). A velocidade da reação direta diminui com o tempo, devido ao decréscimo de reagentes (menor número de choques efetivos). Ao mesmo tempo, a velocidade da reação inversa aumenta, por causa do aumento da concentração dos produtos.
Finalmente, em t3, a velocidade da reação direta diminui e a da reação inversa aumenta, a ponto de se igualarem. A partir daí não há mais variação das concentrações de reagentes e produtos, uma vez que estes são formados e consumidos em velocidades iguais:
CO2 (g) + H2 (g) ![]() CO(g) + H2O(g)
CO(g) + H2O(g)
A constante de equilíbrio
Considere a seguinte reação genérica: aA + bB ![]() cC + dD. Chamaremos as velocidades das reações direta e inversa de V1 e V2, respectivamente. As equações que representam essas velocidades são:
cC + dD. Chamaremos as velocidades das reações direta e inversa de V1 e V2, respectivamente. As equações que representam essas velocidades são:
V1 = K1 [A]a [B]b
V2 = K2 [C]c [D]d
K1 e K2 são as constantes de velocidade, também chamadas constantes cinéticas, das reações direta e inversa, respectivamente. No equilíbrio dinâmico, temos que V1 = V2, ou seja: K1 [A]a [B]b = K2 [C]c [D]d. Desta relação, resulta que:
|
|
Ke é a constante de equilíbrio, e seu valor só é constante a uma temperatura determinada. Variando-se a temperatura, o valor da constante se altera. A partir do valor de Ke, pode-se ter uma idéia do rendimento de uma reação: um valor grande de Ke indica um alto rendimento, já que, pela definição, Ke é a relação entre as concentrações dos produtos e as concentrações dos reagentes; logo, quanto maior o valor de Ke maior deverá ser o valor do numerador (produtos) em relação ao denominador (reagentes). Isto signififca que a quantidade dos produtos formada no final da reação (equilíbrio) é superior à de reagentes remanescentes.
Equilíbrios ácido-base
A dissociação de ácidos fracos:
Sabemos que os ácidos fortes são aqueles que, em solução aquosa, têm praticamente 100% de suas moléculas dissociadas em íons. A porcentagem de moléculas não dissociadas é desprezível. Já os ácidos fracos não se dissociam totalmente. Assim, para estes últimos é possível calcular uma constante que irá relacionar a quantidade de moléculas dissociadas e a quantidade de moléculas não-dissociadas, quando o sistema atinge o equilíbrio. Essa constante de equilíbrio é chamada de constante de dissociação (Kd), e, como estamos tratando de ácidos, a chamaremos de Ka. No caso de ácidos fortes, não faz sentido esse tipo de relação, já que praticamente 100% de suas moléculas estão dissociadas.
A equação proposta por Arrhenius para a dissociação de um ácido HA é: HA(aq) ![]() H+(aq) + A-(aq)
H+(aq) + A-(aq)
Já a equação proposta por Brönsted-Lowry enfatiza o fato do ácido transferir um próton para a água:
HA(aq) + H2O(l) ![]() H3O+(aq) + A-(aq)
H3O+(aq) + A-(aq)
A condição desse equilíbrio é escrita como [H3O+][A-] / [HA][H2O]. No entanto, como a concentração de moléculas de água permanece constante, ou seja, não influi nos cálculos da equação HA ![]() H+ + A-, o equilíbrio pode ser escrito como [H+][A-] / [HA]. Isto seria o mesmo que considerar o íon H3O+ apenas como H+ (que é a espécie que realmente importa), mas como não existe o próton na sua forma livre, devemos saber que H+ está sob a forma de H3O+. Portanto, a constante de dissociação (Ka) para um ácido fraco HA pode ser definida como:
H+ + A-, o equilíbrio pode ser escrito como [H+][A-] / [HA]. Isto seria o mesmo que considerar o íon H3O+ apenas como H+ (que é a espécie que realmente importa), mas como não existe o próton na sua forma livre, devemos saber que H+ está sob a forma de H3O+. Portanto, a constante de dissociação (Ka) para um ácido fraco HA pode ser definida como:
| Ka = [H+][A-] / [HA] |
A força de um ácido, isto é, seu grau de ionização em solução, é indicada pela magnitude de sua constante de dissociação (Ka). Quanto mais fraco o ácido, menor será o valor de Ka. No caso de ácidos polipróticos, ou seja, ácidos que possuem mais de um hidrogênio ionizável, irão existir mais de uma constante de dissociação. Isto porque a ionização de um ácido poliprótico ocorre em etapas, e cada etapa terá um valor para Ka. Veja como exemplo o ácido sulfuroso:
H2SO3(aq) + H2O(l) ![]() H3O+(aq) + HSO3-(aq) Ka1 = 1,3 x10-2
H3O+(aq) + HSO3-(aq) Ka1 = 1,3 x10-2
HSO3-(aq) + H2O(l) ![]() H3O+(aq) + SO32-(aq) Ka2 = 6,3 x 10-8
H3O+(aq) + SO32-(aq) Ka2 = 6,3 x 10-8
Podemos generalizar que a saída de um próton de um ácido poliprótico torna-se cada vez mais difícil, ou seja, o primeiro próton é liberado com mais facilidade em relação ao segundo e assim, sucessivamente (perceba que o valor de Ka diminui). Isto ocorre porque, com a saída do primeiro próton, a base conjugada tende a recapturar o próton cedido, simultaneamente à saída do segundo.
A dissociação de bases fracas:
A dissociação de uma base fraca em solução aquosa é semelhante à de um ácido fraco, exceto pelo fato de que a atenção é focalizada para a produção de íons OH-. Se considerarmos uma base fraca BOH qualquer, pela definição de Arrhenius a sua dissociação será escrita como: BOH(aq) ![]() B+(aq) + OH-(aq)
B+(aq) + OH-(aq)
Já a equação proposta por Brönsted-Lowry enfatiza o fato da base agir como receptora de um próton da água:
BOH(aq) + H2O(l) ![]() BH+(aq) + OH-(aq)
BH+(aq) + OH-(aq)
A condição do equilíbrio é escrita como [BH+][OH-] / [BOH]. Portanto, a constante de dissociação para uma base fraca BOH (chamamos de Kb) pode ser definida como:
| Kb = [BH+][OH-] / [BOH] |
Podemos abordar um caso interessante, envolvendo a substância amônia (NH3). À temperatura e pressão ambientes a amônia é um gás muito solúvel em água, com a qual forma uma solução básica. Acreditava-se, no passado, que a amônia reagia com a água formando uma base fraca de Arrhenius, de fórmula NH4OH (hidróxido de amônio). Apesar de hoje em dia ainda se considerar uma solução aquosa de amônia como hidróxido de amônio, sabe-se que moléculas NH4OH não existem, pois elas não só não podem ser isoladas como substância pura, como também pode ser demonstrado que estas moléculas não existem nem em solução. Por isso, a amônia é tratada como uma base de Brönsted-Lowry:
NH3(aq) + H2O(l) ![]() NH4+(aq) + OH-(aq)
NH4+(aq) + OH-(aq)
Para essa reação a condição do equilíbrio (Kb) é: [NH4+][OH-] / [NH3]
