O ácido acetilsalicílico (AAS) é um importante composto do ponto de vista farmacológico, conhecido por aspirina.
Material necessário:
Balão de fundo redondo 250 mL
Béquer 500 mL
Pipeta e pêra
Kitassato
Funil de Buchner
Erlenmeyer
Ácido sulfúrico concentrado (H2SO4)
Anidrido acético (C4H6O3)
Carvão ativo
Procedimento experimental:
Coloque no balão seco 2 g de ácido salicílico e 4 mL de anidrido acético. Adicione à mistura 2 gotas de ácido sulfúrico concentrado, que servirá como doador de próton, para processar a reação mais rapidamente. Agite a mistura e aqueça-a em banho-maria à temperatura de 50-60oC durante 15 minutos. Retire a mistura do banho-maria e deixe-a esfriar até a temperatura ambiente, agitando ocasionalmente. Adicione 20 mL de água destilada fria e agite bem. Filtre a vácuo e lave com água gelada. Faça a recristalização do material. A aspirina pode ser recristalizada com uma mistura de etanol e água (proporção 3:7). OBS: A acetilação do ácido salicílico pode ser feita com cloreto de etanoíla (haleto de ácido), em vez de anidrido acético.
Mecanismo da reação:
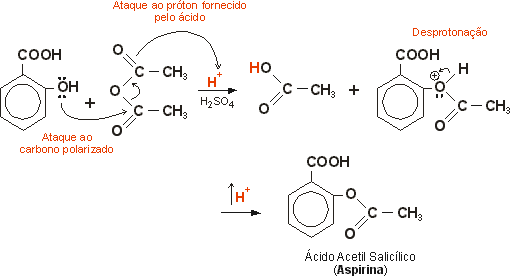
Identificação e hidrólise da aspirina:
Pode-se fazer um teste bastante eficaz para verificar se o ácido salicílico foi totalmente consumido, ou seja, se não existem resíduos desse ácido junto ao produto (aspirina). Isso pode ajudar a determinar o grau de pureza do composto sintetizado. Transfira a aspirina, previamente triturada, e dissolva-a em um tubo de ensaio contendo 3 mL de etanol. Com uma pipeta, pegue 3 gotas dessa solução e coloque num outro tubo de ensaio, misturando com 1 ou 2 gotas de cloreto férrico (FeCl3), que possui uma coloração amarelada: Se a cor da solução permanecer amarela, significa que a síntese teve um bom rendimento. Uma coloração violeta indicará a presença de hidroxilas fenólicas, ou seja, o ácido salicílico ainda existe na mistura, o que significa que o rendimento foi baixo.
Considerando que a aspirina esteja pura, adicione ao tubo que contém o restante dela 2 mL de hidróxido de sódio (NaOH) a 10% e aqueça por 5 ou dez minutos em banho-maria (60 – 70oC). Esta é a reação de hidrólise da aspirina. Depois de retirar o tubo, acidifique com 3 mL de ácido sulfúrico a 10% e resfrie a mistura introduzindo o tubo em água gelada. Separa por filtração em funil de Buchner o sólido formado. Nesta etapa, muitas vezes obtém-se apenas pequena quantidade de sólido. Se isto acontecer, filtre novamente. teste o sólido obtido quanto à presença de fenóis.
Veja abaixo o esquema do mecanismo da reação de hidrólise da aspirina:
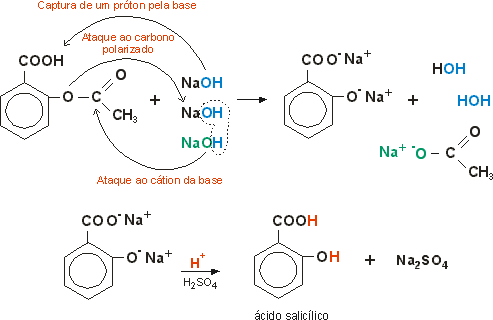
QUESTIONÁRIO
1. Escrever a equação da reação de obtenção da ASPIRINA.
2. Que tipo de reação se verifica na obtenção da ASPIRINA?
3. Qual a finalidade da adição de ácido sulfúrico concentrado?
4. Por que, na determinação do ponto de fusão da ASPIRINA, não se encontra um valor real?
5. Calcular o rendimento teórico de ASPIRINA se 1,0 kg de ácido salicílico é usado com 2,0 kg de anidrido acético?
6. Quais as principais mudanças observadas no espectro de infravermelho do ácido salicílico quando comparado ao espectro do ácido acetilsalicílico?
BIBLIOGRAFIA
MANO E.B.; SEABRA, A.P. Práticas de química orgânica. 3. ed, São Paulo, Edgard Blücher LTDA, 1987.
ALLINGER, N. L.; CAVA, M. P.; JONG, D. C. de; et al. Química orgânica. 2. ed., Rio de Janeiro, Guanabara Dois. 1976.
SILVERSTEIN, R.M.; BASSLER, G.C.; MORRIL, T.C., Identificação espectrométrica de compostos orgânicos. 5. ed, Rio de Janeiro, Guanabara Koogan S. A. 1994.
