Quando a susbtância iodo, que é constituída por moléculas de I2, se encontra no estado sólido, as moléculas estão unidas por interações intermoleculares do tipo dipolo instantâneo-dipolo induzido formando um retículo cristalino molecular.
A figura abaixo representa duas moléculas de I2 vizinhas nesse cristal de iodo sólido. Experimentalmente, verifica-se que a distância entre dois núcleos de iodo que pertençam à mesma molécula (isto é, que estejam unidos por ligação covalente) é de 266 pm*.
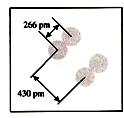
Metade dessa distância é denominada RAIO COVALENTE do iodo.
.jpg)
Ainda considerando a figura, a distância entre dois núcleos de átomos de iodo vizinhos, que não façam parte da mesma molécula, é de 430 pm. A metade de tal dist^ncia é chamada de RAIO DE VAN DER WAALS.
.jpg)
Os valores do raio covalente estão relacionados ao quanto os átomos se aproximam ao fazer uma ligação covalente. Já o raio de Van Der Waals tem a ver com a proximidade de moléculas (unidas por interações intermoleculares), que formam um retículo cristalino molecular.
Em outras palavras, raio covalente é a distância núcleo-núcleo entre átomos numa mesma molécula. Já o raio de Van Der Waals é a distância entre núcleos de átomos em moléculas diferentes pertencentes a mesma substância.
*pm = 10-12 metros
