
Radioatividade é a emissão espontânea de partículas e/ou radiações de núcleos instáveis buscando a estabilidade.
A radioatividade ou radiatividade é um fenômeno natural ou artificial, pelo qual algumas substâncias ou elementos químicos chamados radioativos, são capazes de emitir radiações, as quais têm a propriedade de impressionar placas fotográficas, ionizar gases, produzir fluorescência, atravessar corpos opacos à luz ordinária, etc. As radiações emitidas pelas substâncias radioativas são principalmente partículas alfa, partículas beta e raios gama. A radioatividade é uma forma de energia nuclear, usada em medicina (radioterapia), e consiste no fato de alguns átomos como os do urânio, rádio e tório serem “instáveis”, perdendo constantemente partículas alfa, beta e gama (raios-X). O urânio, por exemplo, tem 92 prótons, porém através dos séculos vai perdendo-os na forma de radiações, até terminar em chumbo, com 82 prótons estáveis.
A radioatividade pode ser:
• Radioatividade natural: É a que se manifesta nos elementos radioativos e nos isótopos que se encontram na natureza.
• Radioatividade artificial ou induzida: É aquela que é provocada por transformações nucleares artificiais.
É importante que o aluno domine as características atômicas e lembre-se de conceitos importantes, tais como:
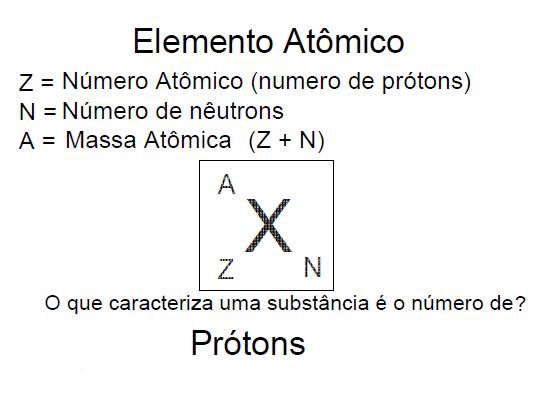

►Radiações Ionizantes – Radioatividade
.jpg)
.jpg)
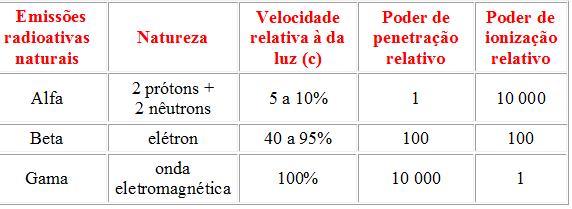
► Natureza das radiações emitidas
As radiações alfa e beta são constituídas, respectivamente, de partículas ![]() e
e ![]() .
.
Partículas ![]() :
:
.jpg)
• têm carga (positiva) + 2, ou seja, o dobro da de 1 próton;
• têm massa 4 (idêntica á dos núcleos de hélio (He – 2 prótons e 2 nêutrons);
• são emitidas com grande velocidade (até um máximo de 30 000 km/s);
• possuem grande energia, sendo porém barradas por uma folha de papel ou por uma lâmina de alumínio de 0,1 mm de espessura;
• têm grande capacidade de ionizar gases (por remoção de elétrons deles).
Partículas ![]() :
:
.jpg)
• têm carga (negativa) -1;
• são elétrons emitidos pelo núcleo dos átomos;
• são emitidas a velocidades muito altas, podendo chegar até próximo da velocidade da luz (300 000 km/s);
• têm poder de penetração maior que as partículas alfa , sendo barradas por placas de a1uminio de 5 mm de espessura ou de chumbo de 1 mm de espessura.
Radiações ![]() :
:

• não têm carga elétrica;
• são radiações semelhantes aos raios X, possuindo, porém, maior energia e menor comprimento de onda (= 0,5 a 100 pm);
• têm velocidade igual à da luz (como todas as ondas eletromagnéticas);
• têm grande poder de penetração, superior até a 15 cm de espessura no aço.
►Leis da Radioatividade
1ª Lei: Soddy
Quando um átomo emite uma partícula α, o seu número atômico diminui de 2 unidades e o seu número de massa diminui de 4 unidades.
90Th232 → +2α4 + 88Ra228
228 + 4 = 232
88 + 2 = 90
2ª Lei: Soddy, Fajans, Russel
Quando um átomo emite uma partícula β, o seu número atômico aumenta de 1 unidade e o seu número de massa permanece inalterado.
90Th234 → -1β0 + 91Pa234
Exemplo:
Dada a equação:
90X204 → x α + y β + 92Y192
Determinar x e y
Resolução:
90X204 → x+ 2α4 + y -1β0 + 92Y192
Montamos duas equações:
a) uma para os índices superiores:
204 = 4x + 0y + 192 ⇒ x = 3
b) uma para os índices inferiores:
90 = 2x + (-1y) + 92
90 = 2(3) -1y +92 ⇒ y = 8
90X204 → 3+ 2α4 + 8 -1β0 + 92Y192
► CINÉTICA DA RADIOATIVIDADE
A velocidade de desintegração ou atividade radioativa não depende de fatores externos como pressão e temperatura, nem da substância sob a qual se apresenta o elemento radioativo. Só depende do número de átomos do elemento radioativo presentes na amostra.
► Meia vida ou período de semidesintegração (P ou t1/2) ⇒
É o tempo necessário para desintegrar metade dos dos átomos radiotaivos de uma amostra.
.jpg)
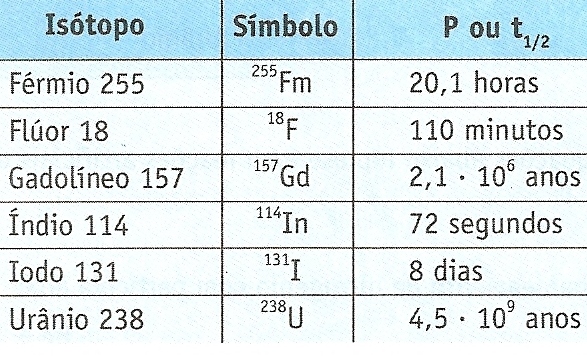
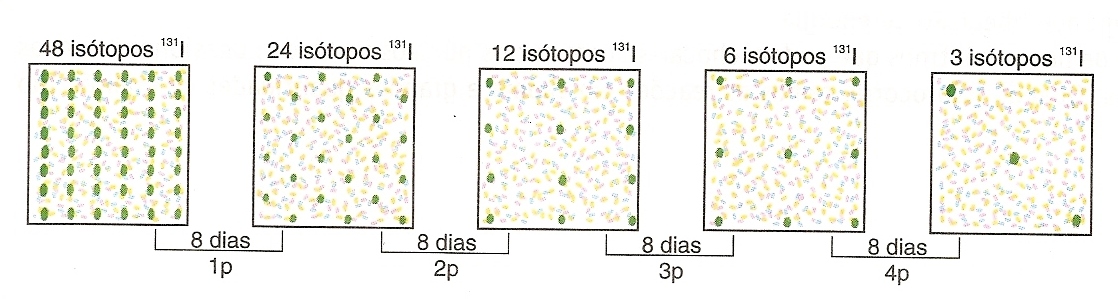
Observe abaixo uma amostra que contém 48 átomos de iodo 131 (I131) e seu gráfico que relaciona os radioisótopos existentes com o número de meias-vidas transcorridas.
.jpg)
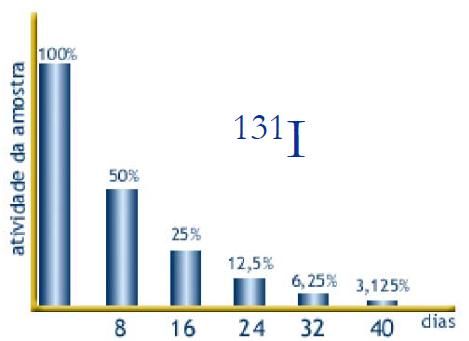
A curva de decaimento acima é característica e serve para o estudo de vários isótopos radioativos existentes, devendo-se verificar apenas a meia-vida de cada um deles.
O número de isótopos radioativos em uma amostra pode ser calculado pela fórmula:
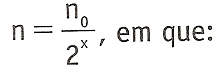
no = o número de átomos no estado inicial
n = número de átomos no estado final
x = número de meias-vidas transcorridas
OBS.: Quando o número de meias-vidas aumenta de 1, 2, 3, 4 vezes etc., o valor da massa inicial (m0) diminui, respectivamente, de 21, 22, 23, 24 etc.
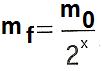
x = é o número de meias-vidas transcorrido.
UM EXEMPLO DOMÉSTICO
Um exemplo “caseiro” pode mostrar bem o conceito de meia-vida, Uma família de 4 pessoas tinha 4kg de açúcar para o consumo normal. Logicamente, a função do açúcar é adoçar o café, o refresco, bolos e sucos. Adoçar é a atividade do açúcar, assim como a emissão de radiação é a atividade dos elementos radioativos.
Por haver falta de açúcar no supermercado, foi preciso fazer um racionamento, até a situação ser normalizada, da seguinte forma: na primeira semana, foram consumidos 2 kg, metade da quantidade inicial, e CONSEGUIU-SE fazer dois bolos, um pudim, refrescos, sucos, além de adoçar o café da manhã.
Na segunda semana, foi consumido 1 kg, metade da quantidade anterior e 114 da inicial. Ai, já não deu para fazer os bolos
Na terceira semana, só foi possível adoçar os refrescos, sucos e café, com os 500 gramas então existentes.
Procedendo da mesma forma, na décima semana restaram cerca de 4 gramas de açúcar, que não dariam para adoçar um cafezinho, Essa quantidade de açúcar não faria mais o efeito de adoçar e nem seria percebida.
No exemplo citado, a meia-vida do açúcar é de uma semana e, decorridas 10 semanas, praticamente não haveria mais açúcar, ou melhor, a atividade adoçante do açúcar não seria notada, No entanto, se, ao invés de 4 kg, a família tivesse feito um estoque de 200 kg, após 10 meias-vidas, ainda restaria uma quantidade considerável de açúcar,
Se o racionamento fosse de sal, a meia-vida do sal seria maior, porque a quantidade de sal que se usa na cozinha é muito menor do que a de açúcar. De fato, leva-se muito mais tempo para gastar 4 kg de sal do que 4 kg de açúcar.
O LIXO ATÔMICO
Os materiais radioativos produzidos em Instalações Nucleares (Reatores Nucleares, Usinas de Beneficiamento de Minério de Urânio e Tório, Unidades do Ciclo do Combustível Nuclear), Laboratórios e Hospitais, nas formas sólida, líquida ou gasosa, que não têm utilidade, não podem ser simplesmente “jogados fora” ou “no lixo”, por causa das radiações que emitem. Esses materiais, que não são utilizados em virtude dos riscos que apresentam, são chamados de Rejeitos Radioativos. Na realidade, a expressão “lixo atômico” é um pleonasmo, porque qualquer lixo é formado por átomos e, portanto, é atômico. Ele passa a ter essa denominação popular, quando é radioativo.

Dica: Para aprofundar seu conhecimento, baixe a lista de exercícios sobre RADIOATIVIDADE na parte de MALHANDO A MENTE (página principal do site).
►Fissão atômica e fusão nuclear
Fissão atômica – Transmutação com divisão do núcleo, dando dois núcleos menores. É a transmutação da bomba atômica.
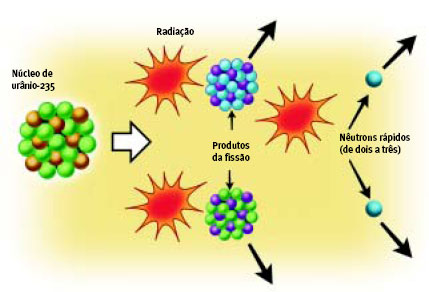
Fusão nuclear – Transmutação com união de dois núcleos, dando um único núcleo. É a transmutação da bomba de hidrogênio.
