1. TIPO DE REAÇÕES:
a) REAÇÕES DE SUBSTITUIÇÃO
Na reação de substituição, um grupo ligado a um átomo de carbono é removido e outro toma o seu lugar. Não há variação no grau de insaturação, isto é, o número de ligantes em torno do átomo de carbono não se altera.
Exemplo:
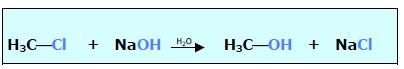
SUBSTITUIÇÃO EM ALCANOS
1. HALOGENAÇÃO (Cl2 ou Br2)
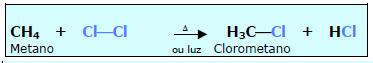
2. NITRAÇÃO (HNO3 = HONO2)
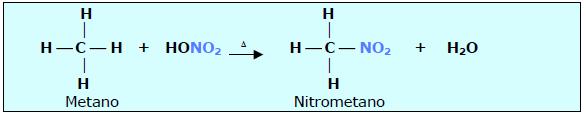
3. SULFONAÇÃO (H2SO4 ou HOSO3H)
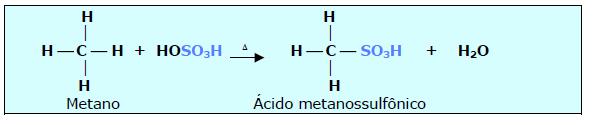
Em alcanos mais complexos a ordem de reatividade dos hidrogênios é:
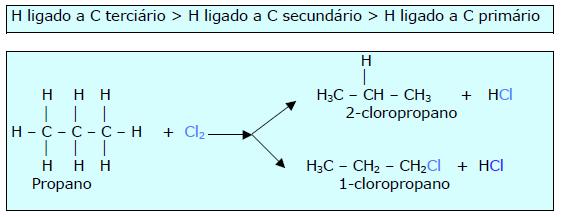
Obs.: Na reação acima forma-se maior quantidade de 2-cloropropano do que 1-cloropropano.
SUBSTITUIÇÃO EM AROMÁTICOS
1. HALOGENAÇÃO (Cl2 ou Br2)
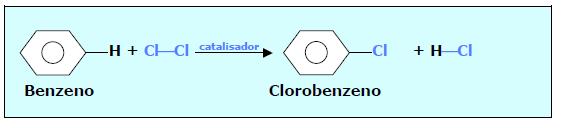
2. ALQUILAÇÃO DE FRIEDEL-CRAFTS
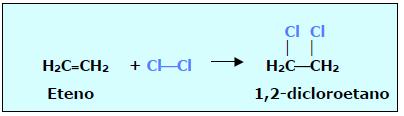
b) REAÇÕES DE ADIÇÃO
Na reação de adição, há um aumento no numero de grupos ligados ao carbono. A molécula torna-se mais saturada.
Exemplo:
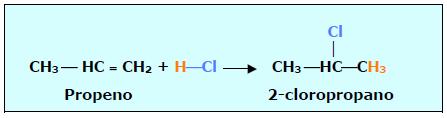
REGRA DE MARKOVNIKOV
Esta regra é aplicada geralmente quando o reagente é HX (HCl, HBr, HI) e H2O.

Exemplo:
REAÇÕES DE ADIÇÃO MAIS USUAIS:
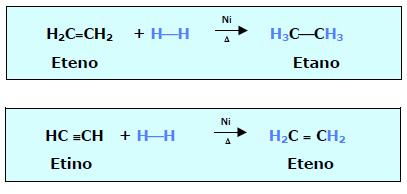
1. HIDROGENAÇÃO CATALÍTICA (ADIÇÃO DE H2)
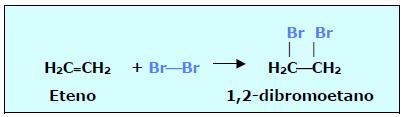
2. HALOGENAÇÃO: (ADIÇÃO DE Cl2 ou Br2)
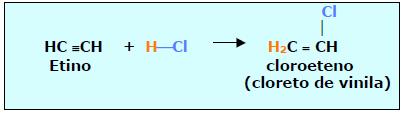
3. ADIÇÃO DE HX (HCl , HBr, HI)
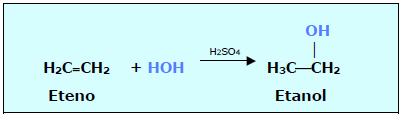
4. HIDRATAÇÃO: (ADIÇÃO DE H2O)
5. ADIÇÃO EM AROMÁTICOS
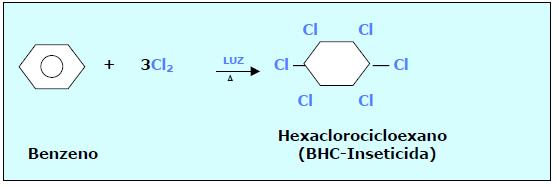
c) REAÇÕES DE COMBUSTÃO
.jpg)
d) REAÇÃO DE ESTERIFICAÇÃO
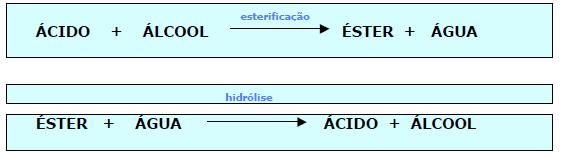
Exemplo:
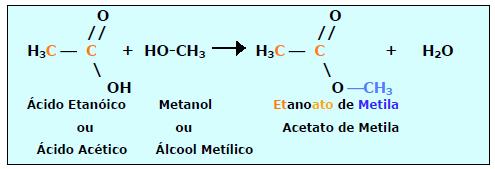
e) SAPONIFICAÇÃO
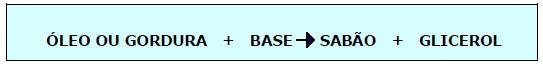
Exemplo:
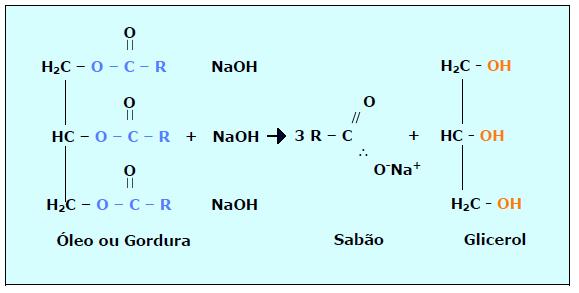
Observação:
Sabão é um sal de ácido graxo, isto é, um sal de ácido carboxílico de cadeia longa. A utilização de NaOH irá originar sabão duro, e quando utilizarmos KOH, obteremos sabão mole. Sabões e detergentes são agentes emulsificantes. Geralmente, o nome detergente é reservado para ácidos sulfônicos e seus derivados.
