- Matéria:
– É tudo aquilo que possui massa e ocupa lugar no espaço. (Ex: madeira, vidro, etc…)
Estados Físicos (ou de Agregação) da Matéria:
a) Sólido: apresenta forma e volume constantes. As forças de atração entre as moléculas prevalecem sobre as forças de repulsão.
b) Líquido: apresenta forma variável e volume constante. As forças de atração e repulsão entre as moléculas são iguais.
c) Gasoso: apresenta forma e volume variáveis. As forças de repulsão entre as moléculas prevalecem sobre as forças der atração.
- Mudanças de Estado de Físico :
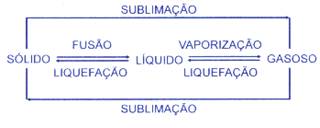
Substâncias e Misturas :
- Substâncias Puras ou Espécies Químicas
São sistemas constituídos por átomos ou moléculas quimicamente iguais. Dividem-se em:
- Substâncias Simples:
– São formadas por átomos de um único elemento químico.
Exemplos: oxigênio (O2), hidrogênio (H2), ferro (Fe)…
b) Substâncias Compostas:
– São formadas por átomos de dois ou mais elementos químicos.
Exemplos: água (H2O), cloreto de sódio(NaCl), carbonato de cálcio (CaCO3).
– Alotropia: Fenômeno em que duas ou mais substâncias simples diferentes são formadas pelo mesmo pelo mesmo elemento químico.
Exemplos: gás oxigênio (O2) e ozônio (O3) – alótropos por atomicidade; grafite e diamante – alótropos por estrutura cristalina.
- Misturas
São sistemas constituídos por duas ou mais substâncias puras. Dividem-se em:
a) Misturas Homogêneas (ou Soluções)
– Apresentam a mesma composição em toda a sua extensão. Apresentam uma única fase.
FASE → Porção homogênea (aspecto uniforme) de um sistema.
Exemplos: solução de água e sal de cozinha, ar atmosférico, bronze (liga de cobre e estanho)
Obs.: substâncias puras e misturas homogêneas são sistemas homogêneos.
b) Misturas Heterogêneas:
– Apresentam diferentes composições em sua extensão. Apresentam mais de uma fase . Às vezes,somente através do microscópio podemos distinguir as suas fases.
Exemplos: areia e cascalho , água e óleo , sangue, leite…
Obs.: substâncias puras durante suas mudanças de estado físico e misturas heterogêneas são sistemas homogêneos.
- Gráficos de Mudança de Estado :
- Substância Pura:
Quando aquecemos ou resfriamos uma substância pura, a pressão constante, a temperatura se mantém constante durante as mudanças de estado físico.
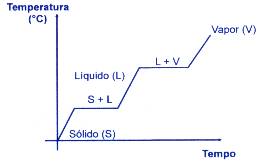
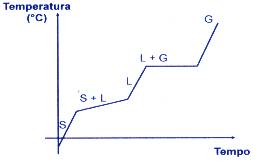
- Mistura:
Quando aquecemos ou resfriamos uma mistura, a pressão constante, a temperatura varia durante as mudanças de estado físico.
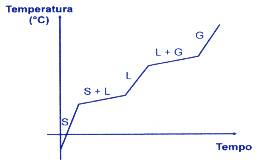
- Mistura Eutética
Comporta-se como substância pura durante a fusão. Exemplo: liga com 62% de Sn e 38% de Pb – solda
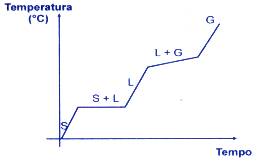
- Mistura Azeotrópica
Comporta-se como uma substância pura durante a ebulição. Exemplo: mistura de 96% de etanol e 4% de água.
Transformações da Matéria :
- Fenômenos Físicos:
São aqueles em que a estrutura da matéria não é alterada. Não promovem a formação de novas substâncias. Exemplos: mudanças de estado físico, filtração, dissolução do cloreto de sódio em água, etc.
- Fenômenos Químicos:
São aqueles em que a estrutura da matéria é alterada. São acompanhados de reações químicas, promovendo a formação de novas substâncias.
Exemplos: ferrugem (oxidação do ferro pelo ar), combustão do etanol, queima da madeira, etc.
Principais Processos de Separação de Misturas (Quadro) :
1 – Precessos utilizados para separação de misturas HETEROGÊNEAS:
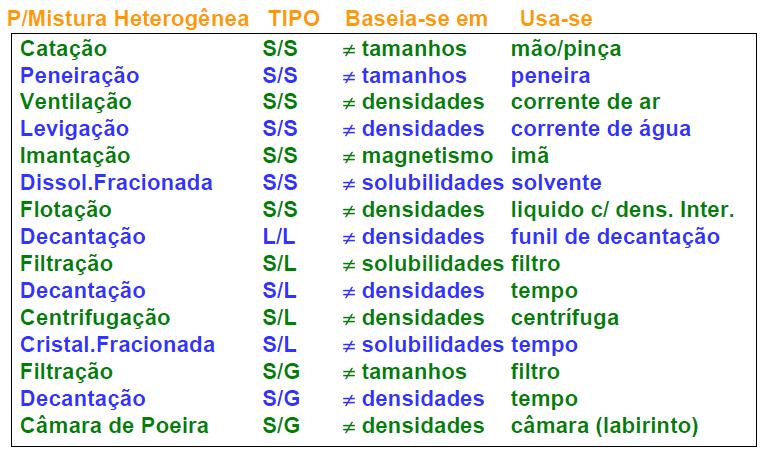
2 – Precessos utilizados para separação de misturas HOMOGÊNEAS:
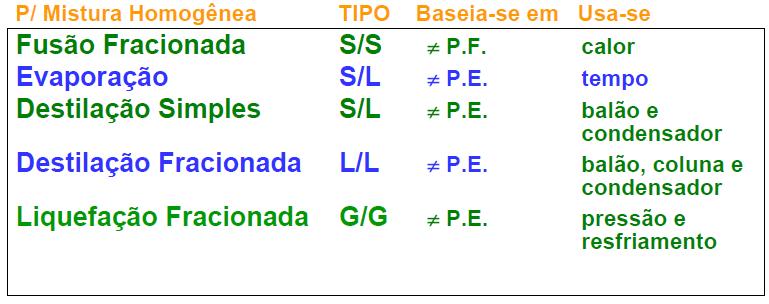
Legenda:
S = sólido L = líquido G = gasoso
