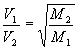Teoria cinética dos gases
Características de uma substância no estado gasoso – Não tem forma e nem volume próprios. Um gás tem a forma do recipiente onde está contido e ocupa todo o espaço limitado pelas paredes do recipiente. O volume de um gás é o volume do recipiente onde está contido.
Modelo do estado gasoso (teoria cinética dos gases) – Um gás é constituído por moléculas isoladas, separadas umas das outras por grandes espaços vazios em relação ao seu tamanho e em contínuo movimento de translação, rotação e vibração.
Pressão e temperatura de um gás
Pressão de um gás – Resulta das colisões das moléculas contra as paredes do recipiente onde está contido.
Temperatura de um gás – É uma medida da agitação molecular ou da agitação térmica.
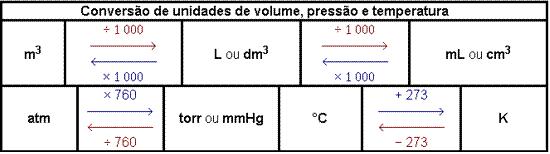
CONVERSÃO DE UNIDADES:
Gás ideal
Gás ideal ou gás perfeito – É um modelo teórico. É um gás que obedece às equações P·V/T = k e P·V = n·R·T, com exatidão matemática.
Na prática, temos gases reais. Um gás real tende para o gás ideal quando a pressão tende a zero e a temperatura se eleva.
CNTP
Condições normais de temperatura e pressão (CNTP)
P = 1,00 atm e T = 273K
| R = 0,082 | atm·L mol·K |
= 62,3 | mmHg·L mol·K |
Lei de Boyle e lei de Charles e Gay-Lussac
Lei de Boyle – A temperatura constante, o volume ocupado por uma quantidade fixa de um gás é inversamente proporcional à sua pressão.
P·V = k = constante
Lei de Charles e Gay-Lussac – A volume constante, a pressão de uma massa fixa de um gás varia linearmente com a temperatura do gás em graus Celsius.
A pressão constante, o volume de uma massa fixa de um gás varia linearmente com a temperatura do gás em graus Celsius.
Com a introdução da escala absoluta, as leis de Charles e Gay-Lussac foram assim enunciadas:
- A volume constante, a pressão de uma massa fixa de gás é diretamente proporcional à temperatura absoluta do gás.
- A pressão constante, o volume de uma massa fixa de gás é diretamente proporcional à temperatura absoluta do gás.
Equação geral dos gases perfeitos
|
(número de mols constante)
|
ISOBÁRICA (P1 = P2) |
|
lei de Charles |
|||
|
ISOCÓRICA |
|
lei de Charles e |
|||
|
ISOTÉRMICA |
P1·V1 = P2·V2 |
lei de Boyle |
Volume molar de um gás
Volume molar é o volume de um mol de substância.
O volume molar de um gás é constante para todos os gases a uma mesma pressão e temperatura.
Nas CNTP, o volume molar é igual a 22,4 L/mol.
Densidade de um gás
Densidade de um gás nas CNTP:
|
Densidade de um gás a uma pressão p e temperatura T:
| d = |
P·M |
Densidade de um gás A em relação a um gás B:
| dA,B = |
MA |
Densidade de um gás A em relação ao ar:
| dA,ar = |
MA |
= |
MA |
Efusão e difusão de gases – Lei de Graham
Efusão de gases é a passagem de gases por pequenos orifícios.
Difusão de gases é a mistura de gases quando colocados uns na presença de outros.
Lei de Graham – As velocidades de efusão e de difusão são inversamente proporcionais às raízes quadradas de suas massas moleculares (ou de suas densidades).